Secuenciación directa de ARN (SQK-RNA004) (DRS_9195_v4_revJ_24Nov2025)
PromethION: Protocol
Secuenciación directa de ARN (SQK-RNA004) V DRS_9195_v4_revJ_24Nov2025
Este protocolo:
- Sirve para secuenciar ARN natural.
- Puede utilizarse con ARN total o una muestra enriquecida —por ejemplo, poli(A) o reducción de ARNr—, como material de entrada inicial.
- No precisa fragmentación.
- Se tarda unos 140 minutos en preparar la biblioteca.
- Es compatible solo con celdas de flujo ARN.
De uso exclusivo en investigación
FOR RESEARCH USE ONLY
Contents
Introducción
Preparación de la biblioteca
Secuenciación y análisis de datos (1)
Descripción general
Este protocolo:
- Sirve para secuenciar ARN natural.
- Puede utilizarse con ARN total o una muestra enriquecida —por ejemplo, poli(A) o reducción de ARNr—, como material de entrada inicial.
- No precisa fragmentación.
- Se tarda unos 140 minutos en preparar la biblioteca.
- Es compatible solo con celdas de flujo ARN.
De uso exclusivo en investigación
1. Aspectos generales
Utilice siempre la versión más reciente del protocolo.
Características del kit Direct RNA Sequencing Kit
Este kit se recomienda a usuarios que:
- Estén explorando características del ARN como bases modificadas.
- A los que les gustaría eliminar sesgos creados por la retrotranscriptasa o la PCR.
- Tienen transcritos que son difíciles de retrotranscribir.
Introducción al protocolo de secuenciación directa de ARN
Este protocolo describe cómo llevar a cabo la secuenciación de una muestra de ARN utilizando el kit de secuenciación Direct RNA Sequencing Kit (SQK-RNA004). A partir de ARN con un apéndice de poli(A) o de ARN total, se sintentiza una segunda cadena de ADNc para ganar estabilidad mediante retrotranscripción. Entonces, se ligan los adaptadores de secuenciación al híbrido ADNc-ARN para secuenciar en celdas de flujo para ARN MinION o PromethION (FLO- MIN004RA / FLO-PRO004RA respectivamente). Nótese, la cadena complementaria de ADNc no se secuencia, pero mejora el resultado de la secuenciación del ARN.
Antes de empezar, se recomienda hacer un experimento de control con RNA Control Strand (RCS) para familiarizarse con la tecnología.
Pasos del proceso de secuenciación:
Preparación del experimento
Pasos:
- Extraer el ARN, evaluar su longitud, cantidad y pureza. Los controles de calidad realizados durante el protocolo son esenciales para garantizar el éxito del experimento.
- Tener a disposición el kit de secuenciación, el instrumental adecuado y los reactivos de otros fabricantes.
- Descargar el programa para obtener y analizar los datos
- Verificar que la(s) celda(s) de flujo tiene(n) suficientes poros para realizar una buena secuenciación.
Preparación de la biblioteca
La tabla siguiente es un resumen de los pasos necesarios en la preparación de la biblioteca.
| Preparación de la biblioteca | Proceso | Tiempo | Parada opcional |
|---|---|---|---|
| Retrotranscripción | Sintetizar la cadena complementaria de ARN | 85 minutos ~ | En esta fase, el ARN retrotranscrito se puede guardar a -80 °C para utilizarse posteriormente. Nótese, esta es la única pausa de este protocolo. |
| Ligación del adaptador y lavado | Ligar los adaptadores de secuenciación a los extremos del híbrido ARN-ADNc | 45 minutos | Ligar los adaptadores de secuenciación a los extremos del híbrido ARN-ADNc. Recomendamos secuenciar la biblioteca tan pronto como se liguen los adaptadores. |
| Acondicionar la celda de flujo y cargar la biblioteca | Acondicionar la celda de flujo y cargar la biblioteca | 10 minutos |

Secuenciación y análisis
Pasos:
- Empezar el proceso de secuenciación usando el programa MinKNOW, que obtendrá datos brutos del dispositivo e identificará las bases.
A diferencia del ADN, el ARN se transloca a través del nanoporo en dirección 3'-5'. Sin embargo, los algoritmos de identificación de bases invierten los datos automáticamente y las lecturas se muestran en dirección 5'-3'.
Compatibilidad de este protocolo
Este protocolo debe utilizarse solo junto con:
- Direct RNA Sequencing Kit (SQK-RNA004)
- PromethION Flow Cell RNA (FLO-PRO004RA)
- Flow Cell Wash Kit (EXP-WSH004) - este kit es adecuado para eliminar la biblioteca entre lavados, pero no eliminará el bloqueo de los poros relacionado con el ARN.
- PromethION™ 24/48 - Requisitos informáticos PromethION
- PromethION™ 2 Solo - Requisitos informáticos PromethION 2 Solo
- PromethION 2 Integrated - [Requisitos informáticos PromethION 2 Integrated] (https://nanoporetech.com/es/document/requirements/promethion-2i-it-req)
We now have available a multiplexing option for direct RNA sequencing: the Direct RNA Barcoding Kit 24 (SQK-DRB004.24)
This kit is suitable for users who have lower output requirements per sample, and want to reduce price-per-sample while streamlining library preparation.
The Direct RNA Barcoding Kit 24 (SQK-DRB004.24) is optimised for use with Poly(A) enriched RNA and IVT samples.
Please visit the Nanopore Store or get in touch with your Oxford Nanopore Technologies representative for more information.
2. Material y consumibles
Material
- 300 ng de ARN con apéndice de poli(A) o 1 µg de ARN total en 8 µl
- Direct RNA Sequencing Kit (SQK-RNA004)
Consumibles
- Celdas de flujo ARN MinION/GridION (FLO-MIN004RA) o celdas de flujo ARN PromethION (FLO-PRO004RA)
- Uno de los siguientes kits: Flow Cell Wash Kit (EXP-WSH004) o Flow Cell Wash Kit XL (EXP-WSH004-XL)
- Induro® Reverse Transcriptase y 5 Induro® RT Reaction Buffer (NEB, M0681)
- 10 mM dNTP solution (e.g. NEB N0447)
- NEBNext® Quick Ligation Reaction Buffer (NEB, B6058)
- Ligasa de ADN T4, 2 M U/ml (NEB, M0202M)
- Inhibidor de RNasa murino (NEB, M0314)
- Agencourt RNAClean XP beads (Beckman Coulter®, A63987)
- Agua sin nucleasas (p.ej. Thermo Scientific, AM9937)
- Etanol al 70 % recién preparado en agua sin nucleasas
- Tubos de PCR de pared fina, 0,2 ml
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Qubit RNA HS Assay Kit (ThermoFisher, Q32852)
- Kit Qubit dsDNA HS (ThermoFisher, Q32851)
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Dispositivos MinION, GridION o PromethION
- Pantalla protectora celdas de flujo MinION/GridION o pantalla protectora celdas de flujo PromethION
- Mezclador vórtex
- Microcentrífuga
- Hula mixer (mezclador de rotación suave)
- Gradilla magnética, adecuada para tubos Eppendorf de 1,5 ml
- Centrifugadora Eppendorf 5424 (o equivalente)
- Cubeta con hielo
- Temporizador
- Termociclador
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P100
- Pipeta y puntas P20
- Pipeta y puntas P10
- Pipeta y puntas P2
En este protocolo necesitará 300 ng de ARN con apéndice de poli(A) o 1 µg de ARN total en 8 µl.
Es posible empezar el protocolo con una cantidad de muestra reducida, aunque tal vez se obtenga un resultado inferior.
Consulte los siguientes gráficos de valoración de muestra inicial a modo de orientación:
ARN con apéndice de poli(A)

ARN total

Muestra inicial de ARN
Es importante que la muestra inicial de ARN posea la cantidad y calidad requerida. Usar demasiado ARN, poco o de mala calidad (p. ej., que esté muy fragmentado o que contenga contaminantes químicos), puede afectar a la preparación de la biblioteca.
Para más información sobre cómo utilizar ARN como muestra inicial, consulte los enlaces a continuación.
- Polyadenylation of non-poly(A) transcripts using E. coli poly(A) polymerase
- RNA contaminants
- RNA stability
- RNA Integrity Number (RIN)
- Enrichment of polyadenylated RNA molecules
Estos documentos pueden encontrarse en la página DNA/RNA Handling
Reactivos de otros fabricantes
Oxford Nanopore Technologies ha probado y recomienda el uso de todos los reactivos de otros fabricantes citados en este protocolo. No se han evaluado otras alternativas.
Recomendamos preparar estos reactivos siguiendo las instrucciones del fabricante.
Verificar la celda de flujo
Antes de empezar el experimento de secuenciación, recomendamos verificar el número de poros disponibles, presentes en la celda de flujo. La comprobación deberá realizarse en las primeras 12 semanas desde su adquisición, si se trata de celdas de flujo MinION, GridION o PromethION. Oxford Nanopore Technologies sustituirá cualquier celda de flujo —no utilizada—, con un número de poros inferior al indicado en la tabla siguiente, siempre y cuando el resultado se notifique dentro de los dos días siguientes a la comprobación y se hayan seguido las instrucciones de almacenamiento. Para verificar la celda de flujo, siga las instrucciones del documento Flow Cell Check.
| Celda de flujo | Número mínimo de poros activos cubierto por la garantía |
|---|---|
| MinION/GridION | 800 |
| PromethION | 5000 |
Contenido del kit Direct RNA Sequencing Kit (SQK-RNA004):
| Nombre | Sigla | Color del tapón | No. de viales | Volumen (μl) |
|---|---|---|---|---|
| RT Adapter | RTA | Azul | 1 | 10 |
| RNA Ligation Adapter | RLA | Verde | 1 | 45 |
| RNA CS | RCS | Amarillo | 1 | 25 |
| Wash Buffer | WSB | Naranja | 2 | 1 200 |
| RNA Elution Buffer | REB | Negro | 1 | 300 |
| Library Solution | LIS | tapón blanco, etiqueta rosa | 1 | 600 |
| Sequencing Buffer | SB | Rojo | 1 | 700 |
| RNA Flush Tether | RFT | Violeta | 1 | 200 |
| Flow Cell Flush | FCF | Blanco | 1 | 8 000 |
Nota: El RNA CS (RCS) es la cadena de control y contiene enolasa II, del gen YHR174W, extraído de la levadura saccharomyces cerevisiae. Los archivos de referencia FASTA, correspondientes a las levaduras, están disponibles aquí.
3. Preparación de la biblioteca
Material
- 300 ng de ARN con apéndice de poli(A) o 1 µg de ARN total en 8 µl
- RT Adapter (RTA)
- RNA CS (RCS)
- Wash Buffer (WSB)
- RNA Ligation Adapter (RLA)
- RNA Elution Buffer (REB)
Consumibles
- Agencourt RNAClean XP beads (Beckman Coulter®, A63987)
- Induro® Reverse Transcriptase y 5 Induro® RT Reaction Buffer (NEB, M0681)
- 10 mM dNTP solution (e.g. NEB N0447)
- NEBNext® Quick Ligation Reaction Buffer (NEB, B6058)
- Ligasa de ADN T4, 2 M U/ml (NEB, M0202M)
- Inhibidor de RNasa murino (NEB, M0314)
- Agua sin nucleasas (p.ej. Thermo Scientific, AM9937)
- Etanol al 70 % recién preparado en agua sin nucleasas
- Tubos de PCR de pared fina, 0,2 ml
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Qubit RNA HS Assay Kit (ThermoFisher, Q32852)
- Kit Qubit dsDNA HS (ThermoFisher, Q32851)
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Mezclador vórtex
- Microcentrífuga
- Termociclador
- Hula mixer (mezclador de rotación suave)
- Gradilla magnética
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
- Cubeta con hielo
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P100
- Pipeta y puntas P20
- Pipeta y puntas P10
- Pipeta y puntas P2
- Centrifuga Eppendorf 5424 (o equivalente)
Verificar la celda de flujo
Antes de empezar a preparar la biblioteca, recomendamos verificar la celda de flujo para comprobar que tiene poros suficientes para realizar un buen experimento de secuenciación.
Las instrucciones de comprobación de la celda de flujo están disponibles en el protocolo de MinKNOW.
Preparar los reactivos NEBNext Quick Ligation Reaction Buffer y T4 DNA Ligase de acuerdo con las instrucciones del fabricante, y colocar en hielo:
Descongelar los reactivos a temperatura ambiente.
Centrifugar los viales durante 5 segundos.
Pipetear los reactivos, al menos 10 veces, hasta que se mezclen completamente. Note: NO mezclar en vórtex el vial T4 DNA Ligase.
El tampón, NEBNext Quick Ligation Reaction Buffer, quizás tenga un poco de precipitado. Dejar que alcance la temperatura ambiente y mezclar con la pipeta varias veces para homogeneizarlo; agitar en vórtex durante varios segundos hasta que el reactivo esté completamente mezclado.
En este protocolo, no recomendamos usar Quick T4 Ligase. Hemos descubierto que la ligasa T4 DNA Ligase (2M U/ml NEB M0202M) funciona mejor. Debe utilizarse junto al reactivo Quick Ligation Reaction Buffer (NEB B6058).
Centrifugar brevemente los viales RT Adapter (RTA), RNA CS (RCS) –si se utiliza– y RNA Ligation Adapter (RLA), mezclar con la pipeta y poner en hielo.
Descongelar a temperatura ambiente los tampones Wash Buffer (WSB) y RNA Elution Buffer (REB) y mezclar en vórtex. Centrifugar brevemente y poner en hielo.
Preparar el ARN en agua sin nucleasas:
- Transferir 300 ng de ARN con apéndice de poli(A) o 1 μl de ARN total en un tubos de PCR, de pared fina (0,2 ml).
- Ajustar el volumen a un total de 8 μl con agua sin nucleasas.
- Mezclar golpeando suavemente el tubo con el dedo para evitar cizalladuras indeseadas.
- Centrifugar brevemente.
El uso de RNA CS (RCS) es una medida de control opcional, adecuada en el control de calidad de la preparación de bibliotecas y la resolución de problemas.
Recomendamos incluir RNA CS (RCS) en la preparación de la biblioteca, por motivos de diagnóstico y resolucion de problemas.
Nótese, este método varía ligeramente dependiendo de la concentración de RNA CS (RCS) presente en el kit. Siga el método e indicaciones adecuado para la concentración de RCS:
Hemos aumentado la concentración de los viales RNA CS (RCS), que se encuentran en los nuevos lotes de SQK-RNA004 y EXP-RCS001.
| Lotes RNA004.20.xxxx o anterior | Lotes RNA004.30.0001 o posterior |
|---|---|
| Vial de RNA CS (RCS) de concentracion baja: 15 ng/µl | Vial de RNA CS (RCS) de concentración aumentada: 50 ng/µl |
| Lotes RCS001.10.xxxx o anterior | Lotes RCS001.20.0001 o posterior |
|---|---|
| Vial de RNA CS (RCS) de concentracion baja: 15 ng/µl | Vial de RNA CS (RCS) de concentración aumentada: 50 ng/µl |
Preparar la reacción del adaptador —RT Adapter (RTA)— de la siguiente manera:
Si no se utiliza RNA CS (RCS) en la muestra inicial, sustituya el volumen de RCS en la mezcla de reacción RTA por agua sin nucleasas.
Uso de RNA CS de concentracion aumentada: disponible en lotes RNA004.30.0001 o posterior:
1. En un tubo nuevo de PCR de pared fina (0,2 ml), diluir al RNA CS (RCS) de entrada como se indica a continuación:
| Reactivo | Volumen |
|---|---|
| RNA CS (RCS) | 1 µl |
| Agua sin nucleasas | 2 µl |
| Total | 3 µl |
2. Mezclar con la pipeta al menos 10 veces hasta que esté bien mezclado.
3. En el tubo de PCR de pared fina (0,2 ml) que contiene la muestra de ARN, combinar los reactivos en el siguiente orden:
| Reactivo | Volumen |
|---|---|
| ARN del paso anterior | 8 µl |
| NEBNext Quick Ligation Reaction Buffer | 3 µl |
| RNA CS (RCS) diluido o agua sin nucleasas | 0.5 µl |
| Murine RNase Inhibitor | 1 µl |
| RT Adapter (RTA) | 1 µl |
| T4 DNA Ligase | 1.5 µl |
| Total | 15 µl |
Uso de RNA CS de concentracion reducida: disponible en lotes RNA004.20.xxxx o posterior:
1. En el tubo de PCR que contiene la muestra de ARN, combinar los reactivos en el siguiente orden:
| Reactivo | Volumen |
|---|---|
| ARN | 8 µl |
| NEBNext Quick Ligation Reaction Buffer | 3 µl |
| RNA CS (RCS) o agua sin nucleasas | 0,5 µl |
| Murine RNase Inhibitor | 1 µl |
| RT Adapter (RTA) | 1 µl |
| T4 DNA Ligase | 1,5 µl |
| Total | 15 µl |
Mezclar con la pipeta y centrifugar brevemente.
Incubar la reacción durante 10 minutos a temperatura ambiente.
En un tubo nuevo Eppendorf DNA Lobind de 1,5 ml, combinar los siguientes reactivos para obtener la mezcla de reacción de transcripción inversa:
| Reactivo | Volumen |
|---|---|
| Agua sin nucleasas | 13 µl |
| 10 mM de dNTPs | 2 µl |
| 5 tampón de reacción Induro RT | 8 µl |
| Total | 23 µl |
Transferir la mezcla de reacción con la transcriptasa inversa al tubo de PCR de 0,2 ml, que contiene el ARN ligado al adaptador y mezclar con la pipeta.
Añadir 2 μl de Induro Reverse Transcriptase a la reacción y meclar con la pipeta.
Colocar el tubo en el termociclador e incubar a 60 °C durante 30 min, a 70 °C durante 10 min y poner a 4 °C antes de proceder con el paso siguiente.
Transferir la muestra a un tubo nuevo de 1,5 ml Eppendorf DNA Lobind.
Resuspender las microesferas Agencourt RNAClean XP mediante vórtex.
Añadir 72 μl de microesferas Agencourt RNAClean XP resuspendidas, a la reacción de transcripción inversa y mezclar con la pipeta.
Incubar en el hula mixer (o mezclador rotatorio) durante 5 minutos a temperatura ambiente.
Preparar 200 µl de etanol al 70 %, con agua sin nucleasas.
Centrifugar la muestra y sedimentar en una gradilla magnética. Sin mover el tubo, retirar el sobrenadante con una pipeta.
Sin retirar el tubo de la gradilla, lavar las microesferas con 150 μl de etanol al 70 % recién preparado, tal y como se describe a continuación:
- Añadir 150 µl de etanol al 70 % recién preparado a cada tubo y esperar a que las microesferas sedimenten a un lado del tubo.
- Sin mover la gradilla magnética, girar los tubos 180°. Esperar a que las microesferas se desplacen hacia el imán y formen un sedimento.
- Girar los tubos 180° de nuevo (hasta la posición inicial) y esperar a que las microesferas sedimenten.
Retirar cuidadosamente el etanol con una pipeta y desechar.
Centrifugar brevemente y poner el tubo de nuevo en la gradilla magnética hasta que el eluído se vuelva claro e incoloro. Sin mover el tubo, retirar con una pipeta cualquier residuo de etanol.
Quitar el tubo de la gradilla magnética y resuspender el sedimento en 23 µl de agua sin nucleasas. Incubar durante 5 minutos a temperatura ambiente.
Sedimentar las microesferas en una gradilla magnética, durante al menos 1 minuto, hasta que el eluido se vuelva claro e incoloro.
Extraer 23 µl de eluido y guardarlo en un tubo Eppendorf DNA Lobind de 1,5 ml.
En este momento, la muestra de ARN-RT puede guardarse a -80 °C y utilizarse más adelante.
Nótese, en este protocolo, este es el único punto donde es posible hacer una pausa.
En el mismo tubo Eppendorf DNA LoBind de 1,5 ml, combinar los reactivos en el siguiente orden:
| Reactivo | Volumen |
|---|---|
| Muestra ARN-RT | 23 µl |
| NEBNext Quick Ligation Reaction Buffer | 8 µl |
| RNA Ligation Adapter (RLA) | 6 µl |
| T4 DNA Ligase | 3 µl |
| Total | 40 µl |
Mezclar con la pipeta.
Incubar la reacción durante 10 minutos a temperatura ambiente.
Resuspender las microesferas Agencourt RNAClean XP mediante vórtex.
Añadir 16 μl de microesferas Agencourt RNAClean XP resuspendidas, a la reacción de transcripción inversa y mezclar con la pipeta.
Incubar en el hula mixer (o mezclador rotatorio) durante 5 minutos a temperatura ambiente.
Centrifugar brevemente la muestra y sedimentar en una gradilla magnética. Esperar 5 minutos y cuando el sobrenadante esté claro e incoloro, retirar con una pipeta.
Añadir 150 μl de Wash Buffer (WSB) a las microesferas. Cerrar la tapa del tubo y resuspender el contenido dando suaves golpes al tubo con el dedo. Volver a colocar el tubo en la gradilla magnética, dejar que las microesferas sedimenten durante 5 minutos y cuando el sobrenadante esté claro e incoloro, retirar con una pipeta.
Repetir el paso anterior.
Al agitar las microesferas se obtiene una eliminación más eficaz del adaptador que al añadir solución amortiguadora y aspirarla inmediatamente.
Centrifugar brevemente el tubo y volver a colocarlo en la gradilla magnética hasta que las microesferas hayan sedimentado. A continuación, retirar cualquier resto de Wash Buffer (WSB) con la pipeta.
Retirar los tubos de la gradilla magnética y resuspender cada sedimento en 33 µl de RNA Elution Buffer (REB), dando suaves golpecitos al tubo con el dedo. Incubar durante 10 min a temperatura ambiente.
Sedimentar las microesferas en la gradilla magnética durante 5 minutos, hasta que el eluido se vuelva claro e incoloro.
Retirar y guardar los 33 µl de eluido en un tubo nuevo Eppendorf DNA LoBind de 1,5 ml.
Cuantificar 1 μl de ARN retrotranscrito y adaptado, con ayuda del ensayo de ADN HS y el fluorímetro qubit.
La cantidad de eluido final que se desea recuperar es > 30 ng.
Las cantidades recogidas varían según las diferentes cantidades de muestra y las preparaciones de bibliotecas. No obstante, recomendamos utilizar el volumen completo de ARN para obtener los mejores resultados en la secuenciación.
El ARN retranscrito y adaptado está listo para cargar la celda de flujo.
La biblioteca de ARN debe secuenciarse inmediatamente y no se puede guardar para utilizarse más adelante.
4. Acondicionar y cargar celdas de flujo PromethION
Material
- Sequencing Buffer (SB)
- Library Solution (LIS)
- Flow Cell Flush (FCF)
- RNA Flush Tether (RFT)
Consumibles
- Celdas de flujo PromethION tipo ARN (FLO-PRO004RA)
- Tubos Eppendorf DNA LoBind de 1,5 ml
Instrumental
- Dispositivo PromethION 24/48 o PromethION 2 Solo
- Pantalla protectora celdas de flujo PromethION
- Mezclador vórtex
- Microcentrífuga
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P100
- Pipeta y puntas P20
Este kit es compatible solo con celdas de flujo tipo ARN (FLO-PRO004RA)
Una vez sacadas de la nevera, esperar 20 minutos antes de insertar las celdas de flujo en el dispositivo y así darles tiempo a que estén a temperatura ambiente. En entornos húmedos se puede formar condensación. Inspeccione las clavijas doradas del conector, situadas en la parte superior e inferior de la celda de flujo, en busca de condensación y si la hubiera, límpiela con una toallita sin pelusa. Procure que la almohadilla térmica (color gris oscuro) esté enganchada en la parte posterior.
Descongelar los viales Sequencing Buffer (SB), Library Solution (LIS), RNA Flush Tether (RFT) y un tubo de Flow Cell Flush (FCF) a temperatura ambiente. Agitar en vórtex y centrifugar brevemente.
En un tubo nuevo de 1,5 ml Eppendorf DNA Lobind mezclar los siguientes reactivos. Agitar en vórtex y centrifugar brevemente.
| Reactivos | Volumen por celda de flujo |
|---|---|
| RNA Flush Tether (RFT) | 30 µl |
| Flow Cell Flush (FCF) | 1 170 µl |
| Total | 1 200 µl |
En el PromethION 2 Solo y PromethION 2 Integrated, cargar la(s) celda(s) de flujo de la siguiente manera:
- Colocar la celda de flujo en la placa metálica.
- Deslizar la celda hacia delante, hasta que las clavijas doradas o la placa verde no se vean.

En el PromethION 24/48, cargar la(s) celda(s) en los puertos de acople de la siguiente manera:
- Alinear la celda con el conector, horizontal y verticalmente, antes de insertarla suavemente en su posición.
- Presionar la celda hacia abajo con firmeza hasta que el pestillo encaje y haga clic en la base.


Insertar la celda de flujo en el ángulo equivocado podría dañar las clavijas del PromethION y afectar los resultados de la secuenciación. Si nota que las clavijas del conector están dañadas, contacte con el servicio de asistencia en support@nanoporetech.com.

Antes de cargar la biblioteca, realizar una comprobación de la celda de flujo a fin de evaluar el número de poros disponible.
Este paso puede omitirse si la celda de flujo se ha comprobado con anterioridad.
Para más información, consultar las instrucciones de comprobación de celdas de flujo en el protocolo de MinKNOW.
Deslizar la tapa del puerto de entrada en el sentido de las agujas del reloj.

Tenga cuidado a la hora de extraer solución amortiguadora de la celda de flujo. No retire más de 20-30 μl y asegúrese de que la solución amortiguadora cubra la matriz de poros en todo momento. La introducción de burbujas de aire en la matriz podría dañar los poros de manera irreversible.
Tras abrir el puerto de entrada, aspirar un volumen pequeño con la pipeta para eliminar burbujas de aire:
- Ajustar la pipeta P1000 a 200 µl.
- Insertar la punta en el puerto de entrada.
- Girar la rueda hasta que el dial marque 220-230 µl o hasta que una pequeña cantidad de solución amortiguadora entre en la punta de la pipeta.

Cargar 500 µl de mezcla de acondicionamiento, evitando introducir burbujas de aire. Esperar cinco minutos. Mientras tanto, preparar la biblioteca siguiendo los siguientes pasos del protocolo.

En un tubo nuevo de 1,5 ml Eppendorf DNA LoBind, preparar la biblioteca como se indica a continuación:
| Reactivo | Volumen por celda de flujo |
|---|---|
| Sequencing Buffer (SB) | 100 µl |
| Library Beads (LIB) bien mezcladas antes de usar o Library Solution (LIS), si se utiliza | 68 µl |
| Biblioteca de ADN | 12 µl |
| Agua sin nucleasas | 20 µl |
| Total | 200 µl |
Cargar despacio 500 µl de mezcla de acondicionamiento.

Mezclar la biblioteca suavemente con la pipeta.
Con una pipeta P1000, cargar 200 µl de biblioteca.

Cerrar la tapa del puerto de entrada.

Para obtener resultados de secuenciación óptimos, coloque la pantalla protectora sobre la celda de flujo justo después de cargar la biblioteca.
Recomendamos colocar la pantalla protectora en la celda de flujo y dejarla puesta mientras la biblioteca esté cargada, incluyendo los lavados y pasos de recarga. Retirar la pantalla cuando se haya extraído la biblioteca de la celda de flujo.
Si se ha retirado la pantalla protectora, colocarla de nuevo de la siguiente manera:
- Alinear la pieza de modo que el orificio coincida con la tapa del puerto de entrada. El borde delantero debería asentarse por encima del identificador de la celda de flujo (sin cubrirlo).
- Presionar con firmeza la pantalla alrededor de la tapa. El clip del puerto de entrada se ajustará con un clic por debajo de la tapa.
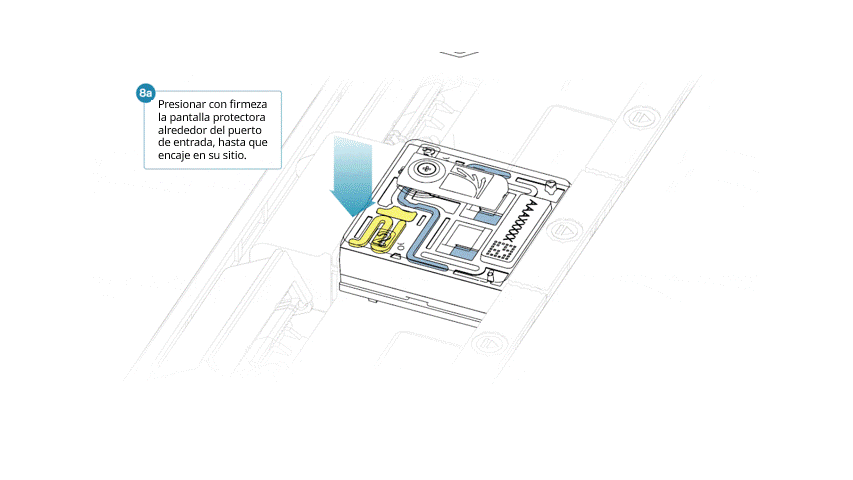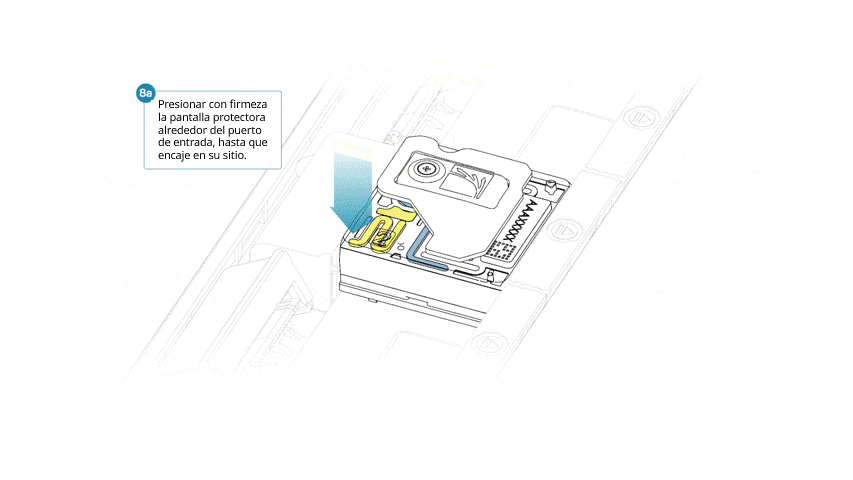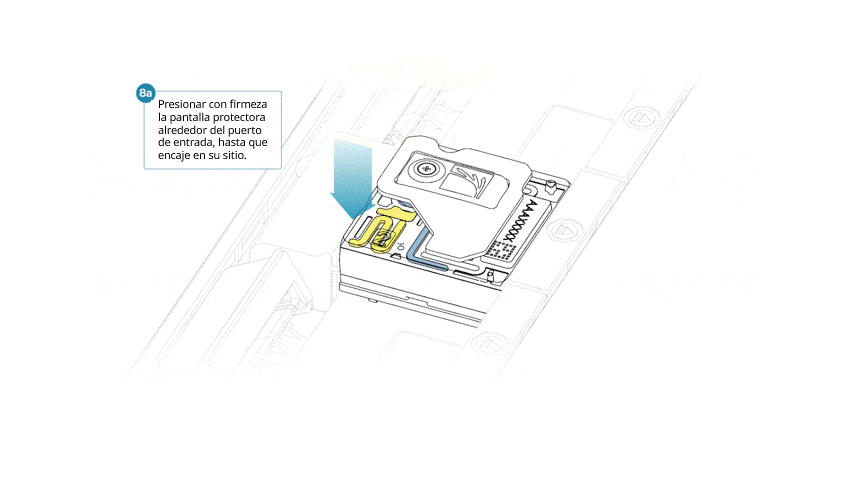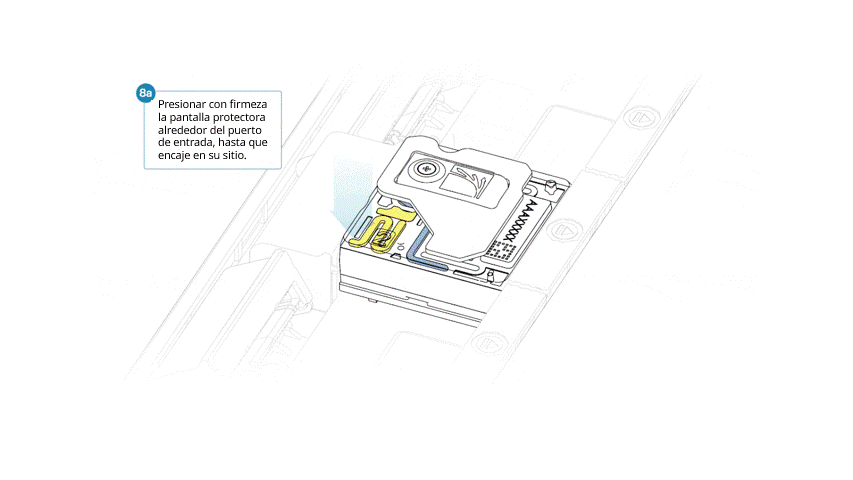

Cerrar la tapa del PromethION cuando esté todo listo para iniciar un ciclo de secuenciación en MinKNOW.
Tras cargar las celdas de flujo, esperar al menos10 minutos antes de iniciar un experimento ayudará a aumentar el rendimiento de la secuenciación.
5. Adquisición de datos e identificación de bases
Cómo empezar a secuenciar
Una vez la celda de flujo esté cargada, el experimento se pone en marcha desde MinKNOW, el programa de secuenciación que gestiona el dispositivo, la adquisición de datos y la identificación de bases en tiempo real. Encontrará intrucciones de uso más detalladas en el protocolo de MinKNOW.
Es posible utilizar y configurar MinKNOW para secuenciar de diferentes maneras:
- En un ordenador conectado a un dispositivo de secuenciación, ya sea directamente o a distancia.
- Directamente desde un dispositivo de secuenciación GridION o PromethION 24/48.
Encontrará más información sobre el uso de MinKNOW en los manuales de usuario de los dispositivos:
- Manual de usuario PromethION 24/48
- Manual de usuario PromethION 2 Solo
- Manual de usuario PromethION 2 Integrated
Cómo empezar un experimento de secuenciación en MinKNOW:
1. Ir a la página principal y pulsar "Iniciar secuenciación".
2. Introducir los datos del experimento, como el nombre, la posición de la celda de flujo y el identificador de la muestra.
3. En la pestaña Kit, seleccionar Direct RNA Sequencing Kit (SQK-RNA004).
4. En la pestaña Configuración del experimento, ajustar los parámetros de secuenciación y salida del experimento o mantener la configuración por defecto.
Nota: Si la identificación de bases estaba desactivada durante la configuración de un experimento, es posible identificar las bases tras la ejecución en MinKNOW. Para más información, consulte el protocolo de MinKNOW.
5. Pulsar Empezar .
Análisis de datos
Una vez la secuenciación haya finalizado, es posible reutilizar o devolver la celda de flujo, como se describe en la sección sobre Reutilización o retorno de celdas de flujo.
Tras secuenciar e identificar las bases, es posible analizar los datos. Si desea más información sobre las opciones de análisis disponible durante y tras la identificación de bases, consulte el documento Data Analysis.
En la sección Análisis, se describen otras opciones para analizar los datos.
6. Reutilización y devolución de celdas de flujo
Material
- Flow Cell Wash Kit (EXP-WSH004) o Flow Cell Wash Kit XL (EXP-WSH004-XL)
El kit Flow Cell Wash Kit (EXP-WSH004 o EXP-WSH004-XL) es compatible con las celdas de flujo de ARN y el kit Direct RNA Sequencing Kit (SQK-RNA004).
No obstante, tenga en cuenta que:
- La DNasa presente en el kit de lavado no ayudará a recuperar los poros bloqueados en la celda de flujo, tras la secuenciación directa de ARN.
- En su lugar, lavará la mayoría de la biblioteca de la matriz y quitará todo el adaptador de la muestra restante, evitando que se vuelva a capturar y secuenciar, lo que permitirá cargar una biblioteca posteriormente.
Si al terminar el experimento desea volver a usar la celda de flujo, siga las instrucciones del protocolo Flow Cell Wash Kit y guarde la celda de flujo lavada a entre 2 °C y 8 ⁰C.
El protocolo Flow Cell Wash Kit está disponible en la comunidad Nanopore.
Una vez terminado el experimento, recomendamos lavar la celda de flujo cuanto antes. Si no es posible, se puede dejar en el dispositivo y lavar al día siguiente.
Otra posibilidad es seguir el procedimiento de devolución, lavar la celda de flujo y enviarla a Oxford Nanopore.
Aquí están las instrucciones para devolver celdas de flujo.
Ante cualquier duda o pregunta acerca del experimento de secuenciación, consulte la sección Resolución de problemas, que se encuentra en la versión en línea de este protocolo.
7. Análisis de datos
Análisis posterior a la identificación de bases
Existen varias opciones para completar el análisis de los datos de bases identificadas:
Flujos de trabajo de EPI2ME
A fin de realizar un análisis en profundidad de los datos, Oxford Nanopore Technologies ofrece una serie de tutoriales sobre bioinformática y flujos de trabajo, que están disponibles en EPI2ME. La plataforma proporciona un espacio donde los flujos de trabajo que depositan en GitHub nuestros equipos de Investigación y Aplicaciones, se pueden exponer con textos descriptivos, código bioinformático funcional y datos de ejemplo.
Herramientas de análisis para la investigación
Para realizar un análisis de datos más exhaustivo, Oxford Nanopore Technologies ofrece una serie de tutoriales y flujos de trabajo bioinformáticos, disponibles en EPI2ME Labs, que encontrará en la sección del mismo nombre de la comunidad Nanopore. La plataforma proporciona un espacio donde los proyectos que depositan en GitHub nuestros equipos de Investigación y Aplicaciones, se pueden exponer con textos descriptivos, código bioinformático funcional y datos de ejemplo.
Herramientas de análisis desarrolladas por la comunidad
Si no se proporciona en ninguno de los recursos anteriores un método de análisis que responda a las necesidades de investigación requeridas, consulte el centro de recursos Resource Centre y busque herramientas bioinformáticas para su aplicación. Varios miembros de la comunidad Nanopore han desarrollado sus propias herramientas y cartera de productos en desarrollo para analizar los datos de la secuenciación por nanoporos. La mayoría de ellas está disponible en GitHub. Oxford Nanopore Technologies no desarrolla ni mantiene esas herramientas y no garantiza que sean compatibles con la última configuración de química/programas informáticos.
8. Problemas durante la extracción de ARN y preparación de la biblioteca
A continuación hay una lista de los problemas más frecuentes, con algunas posibles causas y soluciones propuestas.
También disponemos de una página de preguntas frecuentes, FAQ, en la sección Support de la comunidad Nanopore.
Si ha probado las soluciones propuestas y continúa teniendo problemas, póngase en contacto con el departamento de asistencia técnica, bien por correo electrónico (support@nanoporetech.com) o a través del chat Live Support de la comunidad Nanopore.
Baja calidad de la muestra
| Observaciones | Possibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Baja integridad del ARN (número de integridad del ARN <9,5 RIN o la banda ARNr se muestra como una mancha en el gel) | El ARN se degradó durante la extracción. | Probar un método de extracción de ARN diferente. Para más información sobre el tema, consulte el documento RNA Integrity Number (NIN). Encontrará más información en la página DNA/RNA Handling. |
| El ARN tiene una longitud de fragmento más corta de lo esperado | El ARN se degradó durante la extracción | Para más información sobre el tema, consulte el documento RNA Integrity Number (NIN). Encontrará más información en la página DNA/RNA Handling. Cuando se trabaje con ARN, recomendamos que el ambiente en el que se trabaje, incluido el instrumental de laboratorio, estén libres de ribonucleasas. |
9. Problemas durante la secuenciación de ARN
A continuación hay una lista de los problemas más frecuentes, con algunas posibles causas y soluciones propuestas.
También disponemos de una página de preguntas frecuentes, FAQ, en la sección Support de la comunidad Nanopore.
Si ha probado las soluciones propuestas y continúa teniendo problemas, póngase en contacto con el departamento de asistencia técnica, bien por correo electrónico (support@nanoporetech.com) o a través del chat Live Support de la comunidad Nanopore.
Menos poros al inicio de la secuenciación que tras la evaluación de la celda de flujo
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la evaluación de la celda de flujo | Se introdujo una burbuja de aire en la matriz de nanoporos | Tras comprobar el número de poros presente en la celda de flujo y antes de cebarla, es imprescindible quitar las burbujas que haya cerca del puerto de cebado. Si no se quitan, las burbujas de aire pueden desplazarse a la matriz de nanoporos y dañar de manera irreversible los nanoporos expuestos al aire. La forma más eficaz de evitar que esto ocurra se muestra en los vídeos Cómo cargar celdas de flujo MinION y Cómo cargar celdas de flujo PromethION. |
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la evaluación de la celda de flujo | La celda de flujo no está colocada correctamente | Detener el ciclo de secuenciación, quitar la celda de flujo del dispositivo e insertarla de nuevo. Comprobar que está firmemente asentada en el dispositivo y que ha alcanzado la temperatura deseada. Si procede, probar a colocarla en una posición diferente (GridION/PromethION). |
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la evaluación de la celda de flujo | La presencia de contaminantes en la biblioteca puede haber dañado o bloqueado los poros | El número de poros resultante tras la evaluación de la celda de flujo se realiza usando el control de calidad (CC) de las moléculas de ADN presentes en el tampón de almacenamiento de la celda de flujo. Al inicio de la secuenciación, se utiliza la misma biblioteca para estimar el número de poros activos. Por este motivo, se estima que puede haber una variabilidad del 10 % en el número de poros detectados. Tener un número de poros considerablemente inferior al inicio de la secuenciación puede deberse a la presencia de contaminantes en la biblioteca que hayan dañado las membranas o bloqueado los poros. Para mejorar la pureza del material de entrada, tal vez sea necesario usar métodos de purificación o extracción de ARN alternativos. Los efectos de los contaminantes se muestran en la página Contaminants. Probar con un método de extracción alternativo que no provoque el arrastre de contaminantes. |
Error en el script de MinKNOW
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW muestra el mensaje "Error en el script" | Reiniciar el ordenador y reiniciar MinKNOW. Si el problema continúa, reúna los archivos de registro MinKNOW log files y contacte con el servicio de asistencia técnica. Si no dispone de otro dispositivo de secuenciación, recomendamos que guarde la celda de flujo cargada a 4 °C y contacte con el servicio de asistencia técnica para recibir instrucciones de almacenamiento adicionales. |
Ocupación de poros por debajo del 40 %
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Ocupación de poros inferior al 40 % | No se cargó suficiente cantidad de biblioteca en la celda de flujo | Procure cargar la cantidad de biblioteca de buena calidad recomendada en la preparación de la biblioteca del protocolo correspondiente. Cuantificar la biblioteca antes de cargarla y calcular los moles con herramientas como la calculadora NEBio, opción "RNA ss: mass to moles". |
| Ocupación de los poros próxima a 0 | No hay anclaje en la celda de flujo | Los anclajes se añaden durante el cebado de la celda de flujo (vial FCT) No olvide añadir Flow Cell Tether (FCT) al Flow Cell Flush (FCF) antes del cebado. |
Gran proporción de poros inactivos
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Gran proporción de poros inactivos o poros no disponibles (se muestran en azul claro en el panel de canales y en el gráfico de actividad de poros. Los poros o membranas están irreversiblemente dañados) | Se han introducido burbujas de aire en la celda de flujo | Las burbujas de aire introducidas durante el cebado de la celda y la carga de la biblioteca pueden dañar los poros de manera irreversible. La forma más eficaz de evitar que esto ocurra se muestra en los vídeos Cómo cargar celdas de flujo MinION y Cómo cargar celdas de flujo PromethION. |
| Gran proporción de poros inactivos/no disponibles | Hay contaminantes presentes en la muestra | Los efectos de los contaminantes se muestran en la página Contaminants. Probar con un método de extracción alternativo que no provoque el arrastre de contaminantes. |
Fluctuación de la temperatura
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Fluctuación de la temperatura | La celda de flujo ha perdido contacto con el dispositivo | Comprobar que una almohadilla térmica cubra la placa metálica de la parte posterior de la celda de flujo. Reinsertar la celda de flujo y presionar para asegurarse de que las clavijas del conector estén bien conectadas al dispositivo. Si el problema continúa, contacte con el servicio de asistencia técnica. |
Error al intentar alcanzar la temperatura deseada
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW muestra el mensaje "Error al intentar alcanzar la temperatura deseada" | El dispositivo ha sido colocado en un lugar con una temperatura ambiente inferior a la media o en un lugar con escasa ventilación (lo que provoca el sobrecalientamiento de las celdas de flujo). | MinKNOW dispone de un tiempo predeterminado para que las celdas de flujo alcancen la temperatura fijada. Una vez transcurrido ese tiempo, aparece un mensaje de error, pero el experimento de secuenciación continúa. Secuenciar a una temperatura incorrecta puede provocar disminuciones en el rendimiento y generar índices de calidad Qscore menores. Corrija la ubicación del dispositivo, procurando que esté a temperatura ambiente y tenga buena ventilación; a continuación, reinicie el proceso en MinKNOW. Encontrará más información sobre el control de temperatura del MinION en este enlace. |







