Ligation sequencing DNA V14 (SQK-LSK114) [ライゲーションシークエンシングDNA V14 (SQK-LSK114) ] (GDE_9161_v114_revAC_24Sep2025)
MinION: Protocol
Ligation sequencing DNA V14 (SQK-LSK114) [ライゲーションシークエンシングDNA V14 (SQK-LSK114) ] V GDE_9161_v114_revAC_24Sep2025
- このプロトコールではゲノムDNAを使用します。
- 調製時間は約60分です。
- フラグメンテーションは任意としています。
- PCR無し
- R10.4.1フローセルとの互換性
研究用のみ
この翻訳は英語バージョン「X」をもとに翻訳されています。 新しいバージョンが出ている可能性があるので、この翻訳を使用する前にコミュニティーで今の英語のバージョンをご確認ください。
FOR RESEARCH USE ONLY.
Contents
プロトコールの紹介
ライブラリー調製
シークエンスとデータ解析
トラブルシューティング
概要
- このプロトコールではゲノムDNAを使用します。
- 調製時間は約60分です。
- フラグメンテーションは任意としています。
- PCR無し
- R10.4.1フローセルとの互換性
研究用のみ
この翻訳は英語バージョン「X」をもとに翻訳されています。 新しいバージョンが出ている可能性があるので、この翻訳を使用する前にコミュニティーで今の英語のバージョンをご確認ください。
1. プロトコールの概要
Ligation Sequencing Kit V14 (SQK-LSK114) プロトコルの紹介
このプロトコールは、Ligation Sequencing Kit V14 (SQK-LSK114)を用いたDNAサンプルのシークエンスを行う方法を説明します。この技術に慣れるために、最初にLambdaコントロール実験を行うことを推奨します。
シーケンシングワークフローにおける手順:
実験の準備
実験の前に以下の準備が必要です。
- DNAを抽出し、その長さ、量と純度を確認します。 プロトコル中に実行される品質チェックは実験を成功させるために不可欠です。
- シークエンスキット、適切な装置、およびサードパーティ製試薬が全て揃っていることを確認してください。
- データの取得、および分析するためのソフトウェアをダウンロードしてください。
- フローセルをチェックし、シークエンシングを良好に行うために十分なポアがあることを確認してください。
ライブラリー調製
次の表は、ライブラリー調製手順の概要を示しています。また、オプションで操作を中断できるポイントも示しています。
| ライブラリー調製 | プロセス | 時間 | 停止可能なタイミング(オプション) |
|---|---|---|---|
| DNA修復、およびエンドプレップ | DNAを修復し、DNA末端をアダプターに接続する準備をします。 | 35分 | 4 ° Cで一晩保存 |
| アダプターのライゲーションとクリーンアップ | DNA末端にシークエンスアダプターを取り付けます。 | 20分 | ライブラリーを調製したら、すぐにシークエンスすることを強くお勧めします。 短期間の保管や、フローセルへの再装填など繰り返し使用する場合は、4℃で保管できます。 長期保存、1回使用の場合は-80℃で保存してください。 |
| フローセルのプライミングとローディング | フローセルをプライミングし、調製したライブラリーをシークエンス用にロードします | 5分 |

シークエンシングと解析
実験の事前に以下の手順を行うことが必要です。
- MinKNOWソフトウェアを使用してシークエンスランを開始します。このソフトウェアはデバイスから生データを収集し、リードをベースコールします。
- EPI2MEソフトウェアを起動し、バイオインフォマティクスワークフローを選択してデータを分析します。
プロトコルの互換性
このプロトコルは、以下のものと組み合わせて使用する必要があります。
- Ligation Sequencing Kit V14 (SQK-LSK114)
- Control Expansion (EXP-CTL001)
- R10.4.1 MinION Flow Cells (FLO-MIN114)
- Flow Cell Wash Kit (EXP-WSH004)
- MinION Mk1B - MinION Mk1B IT requirements document
- MinION Mk1C - MinION Mk1C IT requirements document
- MinION Mk1D - MinION Mk1D IT requirements document
- GridION - GridION IT requirements document
2. 機器と消耗品
材料
- 1 µ g(または100 ~ 200 fmol)高分子ゲノムDNA
- または、DNA断片化を行う場合は100 ng以上の高分子ゲノムDNA
- Ligation Sequencing Kit V14 (SQK-LSK114)
消耗品
- MinionとGridIONのFlow Cell
- Qubit dsDNA HS Assay Kit (Invitrogen, Q32851)
- NEBNext® Companion Module v2、Oxford Nanopore Technologies® Ligation Sequencing用 (NEB, E7672S or E7672L)
- nuclease-free waterで調整した 80% エタノール溶液
- Nuclease-free water (e.g. ThermoFisher, AM9937)
- Bovine Serum Albumin (BSA) (50 mg/ml) (e.g Invitrogen™ UltraPure™ BSA 50 mg/ml, AM2616)
- 1.5 ml Eppendorf DNA LoBind tubes
- 0.2 ml 薄壁のPCRチューブ
- Qubit™ Assay Tubes (Invitrogen, Q32856)
装置
- MinIONかGridION のデバイス
- MinIONとGridIONのFlow Cell ライトシールド
- Hula mixer(緩やかに回転するミキサー)
- 1.5 mlエッペンドルフチューブに最適のマグネット式ラック
- 小型遠心機
- ボルテックスミキサー
- サーマルサイクラー
- P1000 ピペット及びチップ
- P200 ピペットとチップ
- P100 ピペットとチップ
- P20 ピペットとチップ
- P10 ピペットとチップ
- P2 ピペットとチップ
- アイスバケツ(氷入り)
- タイマー
- Qubit蛍光光度計(またはQCチェックのための同等品)
DNAサンプルの長さに応じて、サンプル使用量を調整してください
| DNAライブラリー断片長 | サンプルDNA量 |
|---|---|
| 非常に短い (<1 kb) | 200 fmol |
| 短い (1-10 kb) | 100–200 fmol |
| 長い(>10 kb) | 1 µg |
ライゲーションシークエンスプロトコルのサンプル使用量とフローセルへのロード量の詳細については、our know-how documentをご覧ください。
インプットDNA
インプットDNAのQC方法
インプットDNAの量と品質の要件を満たすことが重要です。DNAの使用量が少なすぎたり多すぎたり、あるいは品質の低いDNA(例としてDNAが非常に断片化されていたり、RNAや化学汚染物質が含まれている場合など)を使用すると、ライブラリーの調製に影響を及ぼす可能性があります。
DNAサンプルの品質管理の方法については、Input DNA/RNA QC protocolのプロトコルをご覧ください。
コンタミネーション
DNAの抽出する方法によっては、精製DNAに特定の化学汚染物質が残留する可能性があり、ライブラリ調製の効率やシークエンシングの品質に影響を及ぼす可能性があります。コンタミネーションについての詳細は、コミュニティーの Contaminants page をご覧ください。
Oxford Nanopore Technologies® Ligation Sequencing用のNEBNext® Companion Module v2
NEBNext® Companion Module v2 for Oxford Nanopore Technologies® Ligation Sequencing (catalogue number E7672S or E7672L), を購入されることをお勧めします。この商品にはLigation Sequencing Kitで使用するために必要なすべてのNEB試薬が含まれています。
旧バージョンのNEBNext® Companion Module for Oxford Nanopore Technologies® Ligation Sequencing (NEB, E7180S or E7180L)と互換性がありますが、新しい「モジュールv2」では、FFPEv2 DNA Repair BufferとSalt-T4 DNA Ligaseにより、より効率的なdA-tailingとligationが可能になりました。v2モジュールを使用すると、サンプルあたりのコストを削減できます。
(注: アンプリコンのプロトコールについては、NEBNext FFPE DNA Repair Mixをお買い求めいただくことも可能ですが、試薬を別途でお買い求めいただく方がコスト的に有利です。
サードパーティー試薬
このプロトコールで使用されているすべてのサードパーティー試薬は、当社が検証し、使用を推奨しているものです。Oxford Nanopore Technologiesでは、それ以外の試薬を用いたテストは行っていません。
すべてのサードパーティ製試薬については、製造元の指示に従って使用の準備をすることをお勧めします。
フローセルのチェックをしてください
シークエンシング実験を開始する前に、フローセルのポアの数を確認することを強くお勧めします。このフローセルの確認は、MinION/GridION/PromethIONの場合は代理店への到着から12週間以内に行ってください。またはFlongle Flow Cellの場合は代理店への到着から4週間以内に行う必要があります。Oxford Nanopore Technologiesは、フローセルチェックの実施から2日以内に結果が報告され、推奨される保管方法に従っていた場合に、以下の表に記載されているナノポアの有効数に満たさない場合には、フローセルを交換します。 フローセルのチェックを行うには、Flow Cell Check documentの指示に従ってください。
| Flow cell | 保証する最小有効ポア数(以下の数未満のフローセルが交換対象となります) |
|---|---|
| Flongle Flow Cell | 50 |
| MinION/GridION Flow Cell | 800 |
| PromethION Flow Cell | 5000 |
ライゲーションアダプター(LA)のライゲーション効率を高めるため、NEBNext Quick Ligation Module に付属しているリガーゼバッファーではなく、Ligation Sequencing Kit V14 に付属のライゲーションバッファー(LNB)のご使用を強くお勧めします。
本キットおよびプロトコールに含まれるライゲーションアダプター(LA)は、他のシークエンシングアダプターとの互換性はありません。
Ligation Sequencing Kit V14 (SQK-LSK114) のコンテンツ
(注: 現在のキットの容器を変更しています。今までは実験毎に使い捨てのシングルユーズチューブを使用していましたが、バッファー単位のボトル容器に変更しています。
シングルユースチューブの場合:
ボトル容器の場合:
(注: 本製品には、Beckman Coulter、Inc.製のAMPure XP試薬が含まれており、試薬の安定性を損なうことなくキットと共に-20 ° Cで保存することができます。
(注: DNA Control Sample(DCS)は3.6kbのアンプリコンで、Lambda genomeの3'末端をマッピングしたプレップコントロールです。
3. DNA修復およびエンドプレップ
材料
- 1 µg (又は100-200 fmol) のgDNA
- DNA Control Sample (DCS)
- AMPure XP Beads (AXP)
消耗品
- NEBNext® FFPE DNA Repair Mix (M6630) from the NEBNext® Companion Module v2 (NEB, E7672S or E7672L)
- NEBNext® FFPE DNA Repair Buffer v2 (E7363) from the NEBNext® Companion Module v2 (NEB, E7672S or E7672L)
- NEBNext® Ultra II End Prep Enzyme Mix (E7646) from the NEBNext® Companion Module v2 (NEB, E7672S or E7672L)
- Qubit dsDNA HS Assay Kit (Invitrogen, Q32851)
- Nuclease-free water (e.g. ThermoFisher, AM9937)
- nuclease-free waterで調整した 80% エタノール溶液
- Qubit™ Assay Tubes (Invitrogen, Q32856)
- 0.2 ml 薄壁のPCRチューブ
- 1.5 ml Eppendorf DNA LoBind tubes
装置
- P1000 ピペット及びチップ
- P100 ピペットとチップ
- P10 ピペットとチップ
- 小型遠心機
- サーマルサイクラー
- Hula mixer(緩やかに回転するミキサー)
- マグネットラック
- アイスバケツ(氷入り)
- Qubit™ fluorometer (or equivalent for QC check)
NEB試薬がすべて含まれていまれている Oxford Nanopore Technologies® Ligation Sequencing (catalogue number E7672Sまたは、 E7672L)用のNEBNext® Companion Module v2)を使用する事をお勧めします。
旧バージョンのNEBNext® Companion Module for Oxford Nanopore Technologies® Ligation Sequencing (NEB, E7180S or E7180L)も使用可能です。しかし、上記で推奨したv2モジュールを使用する事でより効率的なdA-tailingとligationを提供できます。
フローセルのチェックを行ってください。
ライブラリー調製を開始する前にフローセルチェックを行い、良好なシークエンスランに十分なポアを持つフローセルを使用することをお勧めします。
詳細については、MinKNOWプロトコルのflow cell check instructions を参照してください。
DNA Control Sample(DCS)を室温で融解し、スピンダウンしてピペッティングで混合し、氷上に置きます。
トラブルシューティングの為、DNAコントロールサンプル(DCS)を自身のライブラリーに添加して、プレップコントロール用に使用することを推奨します。ただし、このステップを省略して、1 µlをサンプルDNAで補うこともできます。
NEB試薬を製造元の指示に従って調製し、氷上に置きます。
最適なパフォーマンスを得るために、NEBは以下を推奨しています。
すべての試薬を氷上で解凍します。
試薬チューブをタッピングや転倒混和にてよく混ぜてください。
(注: FFPE DNA Repair MixまたはUltra II End Prep Enzyme Mixをボルテックスしないでください。毎日、初めて開封する前に、必ずチューブをスピンダウンしてください。
FFPE DNA Repair Buffer v2、または NEBNext FFPE DNA Repair Buffer と Ultra II End Prep Reaction Buffer をボルテックスし、よく混合してください。
(注: これらのバッファーは白色の沈殿を含むことがあります。このような場合には混合物を室温で戻し、バッファー液を数回上下にピペットで沈殿物を分解してください。その後、素早くチューブをボルテックスして混合させてください。FFPE DNA Repair Bufferは黄色味を帯びることがありますが、問題はありません。
ヌクレアーゼを含まない水でDNAを調製します
1μg(または100~200fmol)のインプットDNAを1.5mlのエッペンドルフDNA LoBindチューブに移し替えます。
ヌクレアーゼフリーの水と合計で47 μ lの容量に調製します。
上下にピペッティングをするか、チューブをタッピングする方法で十分に混ぜてください。
小型遠心機を使って、短時間スピンダウンしてください。
0.2 ml 薄壁PCRチューブに以下を混合してください。
それぞれの添加の間に、10~20回ピペッティングして混ぜてください。
| 試薬 | 量 |
|---|---|
| 前ステップのDNA | 47 µl |
| DNA CS(オプション) | 1 µl |
| NEBNext FFPE DNA Repair Buffer v2 | 7 µl |
| NEBNext FFPE DNA Repair Mix | 2 µl |
| Ultra II End-prep Enzyme Mix | 3 µl |
| 合計 | 60 µl |
反応液を完全に混合するために、ゆっくりとピペッティングし短時間スピンダウンして下さい。
サーマルサイクラーを使用して、初めに20℃で5分間インキュベートした後に、65℃で5分間インキュベートしてください。
AMPure XP ビーズ(AXP)をボルテックスで懸濁します。
DNA サンプルを清潔な 1.5 ml エッペンドルフ DNA LoBind チューブに移してください。
再懸濁したAMPure XP Beads (AXP) 60 µlをエンドプレップ反応に加え、チューブをフリッ クして混和します。
Hula mixer(緩やかに回転するミキサー)で5分間インキュベートします(常温)。
新鮮な80%エタノールをヌクレアーゼフリー水で500μl用意します。
チューブをスピンダウンした後、マグネットラック上で、上清が無色透明になるまで置きます。チューブを磁石の上に置いたまま、上清をピペットで取り除いていきます。ピペットを使用してエタノールを除去し 、 廃棄してください。
チューブをマグネットの上に置き、ペレットを乱さないように、200 µl の新しく調製した 80% エタノールでビーズを洗浄します。
前のステップを繰り返します。
スピンダウンし、チューブをマグネットの上に戻します。残ったエタノールをピペットで取り除きます。ペレットを30 秒間程乾かします。 ただし、 ペレットにひびが入るまでは乾燥させないでください。
チューブをマグネットラックから取り出し、ペレットを61μlのヌクレアーゼフリー 水に懸濁します。室温で2分間インキュベートします。
溶出液が無色透明になるまで、少なくとも1分間マグネット上でビーズをペレット化します。
61μlの溶出液を除去し、清潔な1.5mlエッペンドルフDNA LoBindチューブに保持します。
Qubit蛍光光度計を使用して、溶出したサンプル1 µlを定量します。
エンドプレップと修復されたDNAをアダプターライゲーションのステップに進めます。なお、この時点でサンプルを4℃で一晩保存することも可能です。
4. アダプターのライゲーションとクリーンアップ
材料
- Ligation Adapter (LA)
- Ligation Buffer (LNB)
- Long Fragment Buffer (LFB)
- Short Fragment Buffer (SFB)
- AMPure XP Beads (AXP)
- Elution Buffer (EB)
消耗品
- Salt-T4® DNA Ligase (NEB, M0467)
- 1.5 ml Eppendorf DNA LoBind tubes
- Qubit dsDNA HS Assay Kit (Invitrogen, Q32851)
- Qubit™ Assay Tubes (Invitrogen, Q32856)
装置
- マグネットラック
- 小型遠心機
- ボルテックスミキサー
- P1000 ピペット及びチップ
- P100 ピペットとチップ
- P20 ピペットとチップ
- P10 ピペットとチップ
- Qubit蛍光光度計(またはQCチェックのための同等品)
Salt-T4® DNA Ligase (NEB, M0467) の使用を推奨します。
Salt-T4® DNA Ligase(NEB, M0467)は別途購入するか、Oxford Nanopore Technologies® Ligation Sequencing用のNEBNext® Companion Module v2(カタログ番号E7672SまたはE7672L)に含まれています。
旧バージョンのNEBNext® Companion Module for Oxford Nanopore Technologies® Ligation Sequencing (NEB, E7180S or E7180L)も使用することが出来ます。しかし、上記で推奨したv2モジュールを使用する事でより効率的なdA-tailingとligationを提供することが出来ます。
推奨の他社製リガーゼ(ligase)には専用のバッファーが付属していますが、Ligation Sequencing Kitに付属のLigation Buffer (LNB)を使用した方が、Ligation Adapter (LA)のライゲーション効率が高くなります。
Ligation Adapter (LA) とSalt-T4® DNA Ligaseをスピンダウンし、氷上に置きます。
ライゲーションバッファー(LNB)を室温で融解し、スピンダウンしてピペッティングで混合します。粘性が高い為、この緩衝液をボルテックスするのは効果的ではないです。解凍して混ぜたら、すぐに氷の上に置いてください。
溶出バッファー(EB)を室温で融解し、ボルテックスで混合します。その後、スピンダウンして氷の上に置きます。
使用するウォッシュバッファー(LFBまたはSFB)に応じて、アダプターライゲーション後のクリーンアップステップは、3 kb以上のDNAの断片を濃縮するか、全ての断片長を均等に精製するように設計されています。
- 3kb以上のDNA断片を濃縮するには、Long Fragment Buffer (LFB)を使用してください。
- 一方であらゆるサイズの DNA 断片を保持するには、Short Fragment Buffer (SFB) を使用してください。
Long Fragment Buffer(LFB)または Short Fragment Buffer(SFB)のいずれかを室温で解凍し、ボルテックスで混合します。その後、スピンダウンして氷の上に置きます。
1.5mlのエッペンドルフDNA LoBindチューブに、以下の順序で混合してください。
それぞれの添加の間に、10~20回ピペッティングして混ぜてください。
| 試薬 | 量 |
|---|---|
| 前ステップのDNA | 60 µl |
| Ligation Adapter (LA) | 5 µl |
| Ligation Buffer (LNB) | 25 µl |
| Salt-T4® DNA Ligase | 10 µl |
| 合計 | 100 µl |
反応液を完全に混合するために、ゆっくりとピペッティングし短時間スピンダウンして下さい。
反応液を室温で10分間インキュベートします。
AMPure XP ビーズ(AXP)をボルテックスで懸濁します。
再懸濁したAMPure XP Beads (AXP) 40 µlを加え、チューブをフリッ クして混和します。
Hula mixer(緩やかに回転するミキサー)で5分間インキュベートします(常温)。
サンプルをスピンダウンし、マグネット上でペレット化します。チューブをマグネットの上に置き、無色透明になったら上清をピペットで取り除きます。
Long Fragment Buffer(LFB)250 μl、または Short Fragment Buffer(SFB)250 μl を加えてビーズをウオッシュします。タッピングしてビーズを再懸濁させ、スピンダウンします。チューブをマグネットラックに戻し、ビーズをペレット化させます。ピペットで上清を取り除き、廃棄します。
前のステップを繰り返します。
スピンダウンし、チューブをマグネットの上に戻します。残った上清をピペットで取り除きます。ペレットを30 秒間程乾かします。 ただし、 ペレットにひびが入るまでは乾燥させないでください。
チューブをマグネットラックから取り出し、ペレットを15 µlの溶出バッファー(EB)に懸濁します。スピンダウンし、室温で10分間インキュベートして下さい。高分子量のDNAの場合は、37℃でインキュベートすると長い断片の回収率が向上します。
溶出液が無色透明になるまで、少なくとも1分間マグネット上でビーズをペレット化します。
DNA ライブラリーを含む 15 µl の溶出液を取り出し、清潔な 1.5 ml Eppendorf DNA LoBind tube に移し替えます。
ペレット化したビーズを廃棄します。
Qubit蛍光光度計を使用して、溶出したサンプル1 µlを定量します。
DNA ライブラリーの断片サイズに応じて、12 µl の Elution Buffer (EB) で最終のライブラリーを調製します。
| DNAライブラリー断片長 | フローセルローディングの量 |
|---|---|
| 非常に短い (<1 kb) | 100 fmol |
| 短い (1-10 kb) | 35–50 fmol |
| 長い(>10 kb) | 300 ng |
(注: ライブラリーの収量が推奨入力値以下の場合は、ライブラリーの全部の量をロードして下さい。
NEB calculatorなどの計算機を使ってMassとMolの計算をすることを推奨します.
調製されたライブラリーは、フローセルへのロードに使用されます。ライブラリーは、ロードの準備ができるまで氷上、または4℃で保存して下さい。
推奨のライブラリー保存方法
短期間の保存や繰り返し使用する場合は(例 フローセルをウオッシュして再度ロードする場合)は、ライブラリーをEppendorf DNA LoBindチューブに入れ、4℃で保存 することをお勧めします。 __3か月以上の長期保存の場合は、____ライブラリーをEppendorf DNA LoBindチューブに -80 ° Cで保存 することをお勧めします。
5. MinIONおよびGridIONフローセルのプライミングとローディング
材料
- Flow Cell Flush (FCF)
- Flow Cell Tether (FCT)
- Library Solution (LIS)
- Library Beads (LIB)
- Sequencing Buffer (SB)
消耗品
- MinION/GridION Flow Cell
- Nuclease-free water (e.g. ThermoFisher, AM9937)
- Bovine Serum Albumin (BSA) (50 mg/ml) (e.g Invitrogen™ UltraPure™ BSA 50 mg/ml, AM2616)
- 1.5 ml Eppendorf DNA LoBind tubes
装置
- MinIONかGridION のデバイス
- MinION/GridION Flow Cell Light Shields
- P1000 ピペット及びチップ
- P100 ピペットとチップ
- P20 ピペットとチップ
- P10 ピペットとチップ
注意:本キットはR10.4.1フローセル(FLO-MIN114)のみに対応しています。
Take the flow cell out of the fridge and leave it at room temperature for 20 minutes. This will improve visibility of the array during priming and sample loading.
フローセルのプライミングとローディング
新規ユーザーは、 初回使用前に'Priming and loading your flow cell' のビデオをご覧いただくことをお勧めします。
Sequencing Buffer(SB)、Library Beads(LIB)またはLibrary Solution(LISを使用する場合のみ)、Flow Cell Tether(FCT)およびFlow Cell Flush(FCF)を室温で融解してから、ボルテックスで混合します。その後、スピンダウンして氷上で保存します。
MinION R10.4.1フローセル(FLO-MIN114)での最適なシークエンス性能と出力向上のために、フローセルのプライミングミックスに最終濃度0.2 mg/mlでBovine Serum Albumin (BSA) を添加することを推奨します。
(注: その他のアルブミンの種類(組換えヒト血清アルブミンなど)の使用は推奨しません。
BSA入りのフローセルプライミングミックスを調製するには、Flow Cell Flush (FCF)とFlow Cell Tether(FCT)を以下の指示に従って組み合わせます。室温でピペッティングして混合します。
(注: キットの容器を変更している最中です。今までは実験の後に使い捨てるシングルユーズチューブを使用していましたが、バッファー単位のボトル容器に変更しています。お手持ちのキットの使用方法に従ってください。
シングルユースチューブの場合: 50 mg/mlのウシ血清アルブミン(BSA)5 µlとFlow Cell Tether (FCT)30 µlをFlow Cell Flush (FCF)チューブに直接加えます。
ボトル容器の場合:: フローセルの数に適したチューブに以下の試薬を組み合わせます。
| 試薬 | 1フローセルあたりの容量 |
|---|---|
| Flow Cell Flush (FCF) | 1,170 µl |
| Bovine Serum Albumin (BSA) at 50 mg/ml | 5 µl |
| Flow Cell Tether (FCT) | 30 µl |
| 合計 | 1,205 µl |
MinIONまたはGridIONデバイスの蓋を開け、フローセルをクリップの下にスライドさせます。 フローセルをしっかりと押さえ、サーマルプレートと電気接触が密着しているかを確認してください。


ライブラリーをロードする前にフローセルチェックを行い、使用可能なポアの数を把握して下さい。
フローセルが以前にチェックされている場合は、このステップを省略できます。
詳細については、MinKNOWプロトコルのフローセルチェックの手順 flow cell check instructionsを参照してください。
フローセルのプライミングポートカバーを時計方向にスライドさせ、プライミングポートを開きます。

フローセルからバッファーを引き上げる際には注意してください。20~30μl以上は除去せず、ポアのアレイ全体が常にバッファーで覆われていることを確認して下さい。アレイに気泡が入ると、ポアに不可逆的なダメージを与える可能性があります。
プライミングポートを開けた後に、カバーの下に小さな気泡がないかを確認して下さい。気泡を取り除くために少量の液を引き上げます。
- P1000ピペットを200 µ Lに設定して下さい。
- ピペットの先端をプライミングポートに差し込みます。
- 目盛りが220-230 ulと表示されるまでダイヤルを回して、20-30 ulを吸い上げるか、少量のバッファーがピペットの先端に入るのが見えるまでダイヤルを回します。
(注: プライミングポートからセンサーアレイ全体にバッファーがあることを確認してください。

気泡が混入しないように、プライミングポートからフローセルにプライミングミックスを800µl注入し、 5分間待ちます。この5分間の間に、以下の手順でライブラリーをロードする準備をして下さい。

Library Beads(LIB)の液をピペッティングすることで十分に混合して下さい。
Library Beads(LIB)チューブにはビーズの懸濁液が入っています。このビーズはすぐに沈殿するので、使用直前に混合することが重要です。
ほとんどのシークエンシング実験には、Library Beads (LIB)を使用することをお勧めします。しかし、より粘性の高いライブラリーをご使用の場合はLibrary Solution (LIS)の使用をお勧めします。
新しい1.5mlのEppendorf DNA LoBindチューブにてライブラリーをロードする準備をします。(詳細は以下に記載されています。)
| 試薬 | 1フローセルあたりの容量 |
|---|---|
| Sequencing Buffer (SB) | 37.5 µl |
| Library Beads (LIB)またはLibrary Solution(LIS)(使用する場合)は、使用直前に混合して下さい。 | 25.5 µl |
| DNA library | 12 µl |
| 合計 | 75 µl |
フローセルのプライミングを完了させます。
- SpotON サンプルポートカバーをゆっくりと持ち上げ、SpotON サンプルポートにアクセスできるようにします。
- 200μlのプライミングミックスをフローセルのプライミングポート(SpotONサンプルポートではありません)に気泡が入らないように注入します。


調製したライブラリーは、ロードする直前にピペッティング混合して下さい。
調製したライブラリー75μlをSpotONサンプルポートからフローセルに滴下します。次の一滴を追加する前に各一滴がポートに入っていることを確認して下さい。

SpotONサンプルポートカバーをゆっくりと元に戻し、バング(カバーの先)がSpotONポートに入ることを確認し、プライミングポートを閉じます。


最適なシークエンス出力を得るために、ライブラリーがロードされたすぐにライトシールドをフローセルに取り付けてください。
ライブラリーがフローセル上にある状態では(ウォッシングやリロードのステップを含める)、フローセルにライトシールドを付けたままにしておくことを推奨します。ライトシールドは、ライブラリーがフローセルから除去された時点で取り外すことができます。
ライトシールドを以下のようにフローセルに設置して下さい。
ライトシールドの先端を慎重にクリップに当てます。 (注: ライトシールドをクリップの下に無理に押し込まないでください。
ライトシールドをフローセルにゆっくりと下ろします。ライトシールドは、フローセルの上部全体を覆うようにSpotONカバーの周囲に取り付けます。

MinIONフローセルライトシールドは、フローセルに固定されていないため、取り付け後の取り扱いには注意が必要です。
デバイスの蓋を閉め、MinKNOWでシークエンスランをセットします。
When a flow cell is inserted into the MinION Mk1D, the device lid will sit on top of the flow cell, leaving a small gap around the sides. This is normal and has no impact on the performance of the device.
Please refer to this FAQ regarding the device lid.

6. データ収集とベースコール
シークエンスの開始方法
フローセルをロードしたら、MinKNOWでシークエンシングランを開始できます。MinKNOWは、装置、データ収集、リアルタイムベースコールを制御するシークエンスソフトウェアです。 MinKNOWの設定と使用の詳細については、MinKNOW Protocolを参照してください。
MinKNOWは、複数の方法でシークエンスの設定をすることができます。
- シークエンシングデバイスに直接かリモートで接続されているコンピューター。
- GridION、Minion Mk1C、またはPromethion 24/48シークエンシングデバイスで直接使用できます。
シークエンス装置でMinKNOWを使用する方法の詳細については、装置のユーザーマニュアルを参照してください。
MinKNOWでシークエンスランを開始するには、次の手順に従います。
1. スタートページに移動し、 Start sequencing をクリックします。
2. 名前、フローセルの位置、サンプルIDなどの実験の詳細を入力します。
3. キットのページで、ライブラリー調製に使用するシークエンシングキットを選択します。
4. シークエンスランのパラメータの変更を設定(ランオプションの変更など)するか、デフォルト設定のままにします。
(注: シークエンスランの設定時にベースコールがオフになっていた場合には、MinKNOWでポストラン・ベースコールを後日に実行することも出来ます。詳細については、MinKNOW protocolを参照してください。
5. Start をクリックしてシークエンスランを開始します。
シークエンシング後のデータ解析
MinKNOWでシークエンスが終わると、フローセルを再利用または返却ができます。詳しくは、フローセルの再利用と返却のセクションをご覧ください。
シークエンシングとベースコールの後にはデータを解析することができます。 ベースコールおよびベースコール後の解析オプションの詳細については、Data Analysis を参照してください。
ダウンストリーム解析セクションでは、データを解析するためのオプションの概要を説明しています。
7. フローセルの再利用と返却
材料
- Flow Cell Wash Kit (EXP-WSH004)
シークエンス実験終了後、フローセルを再利用する場合は、Flow Cell Wash Kitのプロトコールに従い、洗浄したフローセルを2~8℃で保管してください。
Flow Cell Wash Kit protocolは、Nanoporeコミュニティーで入手できます。
運転を停止したらできるだけ早くフローセルをウォッシュすることをお勧めします。しかし、これが不可能な場合はフローセルをデバイスに入れたまま、翌日にウォッシュをして下さい。
または、返送手順に従って、オックスフォード・ナノポアに返送してください。
フローセルの返却方法は hereをご覧ください。
(注: 製品を返却する前に、すべてのフローセルを脱イオン水で洗浄する必要があります。
シークエンシング実験に関して問題が発生した場合や質問がある場合には、このプロトコルのオンライン版にあるトラブルシューティングガイドを参照してください。
8. ダウンストリーム解析
ベースコール後の分析
ベースコールされたデータをさらに解析するには、いくつかの方法があります。
1. EPI2ME workflows
詳細なデータ解析のために、オックスフォード・ナノポア・テクノロジーズは、EPI2MEで利用可能な様々なバイオインフォマティクスのチュートリアルとワークフローを提供しています。このプラットフォームでは、研究チームとアプリケーションチームがGitHubに保存しているワークフローを記載しています。このプラットフォーム内にはバイオインフォマティクスのコードと説明をしているコメント、およびサンプルデータを使ってコードを試すことが出来ます。
2. 研究分析ツール
Oxford Nanopore Technologiesの研究部門では、Oxford Nanopore GitHub repositoryで多数の分析ツールを公開しています。これらのツールは上級ユーザー向けであり、ソフトウェアのインストールと実行方法の説明が含まれています。これらのツールは最低限のサポートしかしていません。
3. コミュニティーで開発されたツール
研究課題に適したデータ解析方法が上記のリソースのいずれにも記載されていない場合は、 resource centre を参照し、アプリケーションに適したバイオインフォマティクスツールを検索してください。 Nanoporeコミュニティーの多くのメンバーが、 ナノポアシークエンシングデータを解析するための独自のツールやパイプラインを開発しており、そのほとんどはGitHubで利用可能です。これらのツールはOxford Nanopore Technologiesではサポート対象外であり、最新のケミストリーやソフトウェア構成との互換性を保証するものではありませんのでご了承ください。
9. DNA/RNA抽出、およびライブラリ調製時の問題点
以下は、最もよく起こる問題のリストであり、いくつかの原因と解決策が提案されています。
Nanopore Community Support セクションにFAQをご用意しています。
ご提案された解決策を試しても問題が解決しない場合は、テクニカルサポートに電子メール (support@nanoporetech.com)または LiveChat in the Nanopore Communityでご連絡ください。
サンプルの品質が低い
| 問題点 | この問題が生じた可能性のある原因 | 解決策とコメント |
|---|---|---|
| DNAの純度が低い(DNAのOD 260/280のナノドロップ測定値が1.8未満およびOD 260/230が2.0~2.2未満) | DNA抽出で必要な純度が得られていない | 夾雑物の影響は、 Contaminants に示されています。コンタミネーションをもたらさないために別の抽出方法extraction method をお試しください。. 追加のSPRIクリーンアップステップの実施を検討して下さい。 |
| 低いRNA インテグリティー(RNA Integrity Number: <9.5 RIN、またはrRNAバンドがゲル上でスメアになっている) | 抽出中にRNAが分解された | 別のRNA抽出方法 RNA extraction methodを試してください。RINの詳細については、 RNA Integrity Number の資料を参照してください。詳細については、 DNA/RNA Handling のページをご覧ください。 |
| RNAのフラグメントが予想より短い | 抽出中にRNAが分解された | 別のRNA抽出方法 RNA extraction methodを試してください。 RINの詳細については、 RNA Integrity Number の資料を参照してください。詳細については、DNA/RNA Handling のページをご覧ください。 RNAを扱う際には、RNaseフリーの環境で作業し、実験器具もRNaseフリーにしておくことをお勧めします。 |
AMPureビーズクリーンアップ後のDNA回収率が低い
| 問題点 | この問題が生じた可能性のある原因 | 解決策とコメント |
|---|---|---|
| 低回収率 | AMPureビーズとサンプルの比率が予想していたのよりも低いことによるDNAの損失 | 1. AMPureビーズはすぐに沈降するため、サンプルに添加する前によく再懸濁させてください。 2. AMPureビーズ対サンプル比が0.4:1未満の場合、どのようなサイズのDNA断片でもクリーンアップ中に失われます。 |
| 低回収率 | DNA断片が予想よりも短い | サンプルに対するAMPureビーズの比率が低いほど、短い断片に対する選択が厳しくなります。 アガロースゲル(または他のゲル電気泳動法)上でインプットDNAの長さを設定してから、使用するAMPureビーズの適切な量を計算してください。 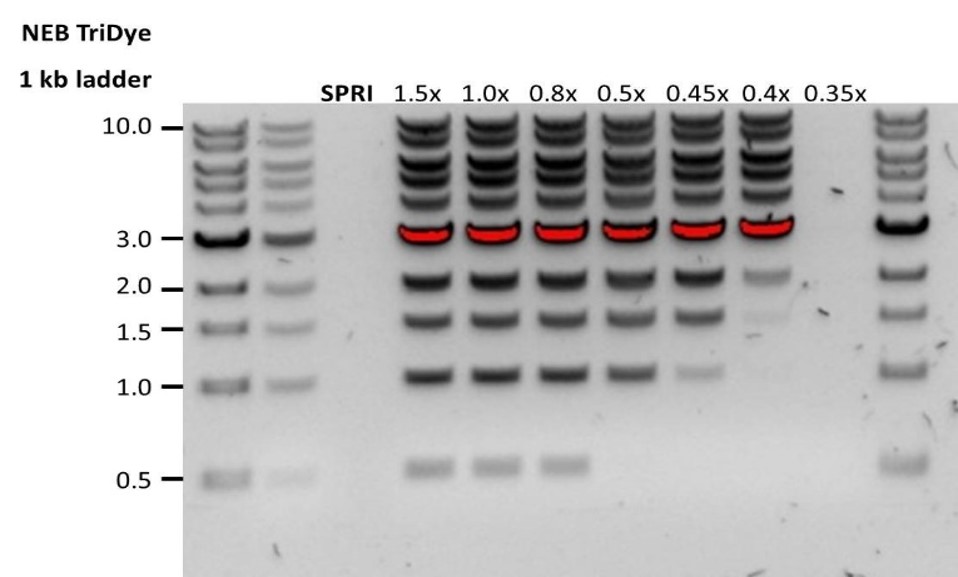 |
| エンドプレップ後の収率が低い | 洗浄ステップで使用したエタノール濃度が低い(70%未満)。 | エタノールが70%未満の場合、DNAは洗浄中にビーズから溶出されます。必ず正しい濃度(%)のエタノールを使用してください。 |
10. シークエンス実行中の問題
以下は、最もよく起こる問題のリストであり、いくつかの原因と解決策が提案されています。
Nanopore Community Support セクションにFAQをご用意しています。
ご提案された解決策を試しても問題が解決しない場合は、テクニカルサポートに電子メール (support@nanoporetech.com)または LiveChat in the Nanopore Communityでご連絡ください。
シークエンス開始時のポアがフローセルチェック後よりも少ない場合
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| MinKNOWのフローセルチェックで確認されたポアの数より、シークエンシング開始時のポア数が少なく表示された。 | ナノポアアレイに気泡が入ってしまった。 | フローセルチェックをした後、フローセルをプライミングする前に、プライミングポート付近の気泡を取り除くことが必要です。 気泡を取り除かないと、気泡がナノポアアレイに移動し、空気に触れたたナノポアが不可逆的なダメージを負った可能性がある。これを防ぐための最適な方法が、 this videoで紹介されています。 |
| MinKNOWのフローセルチェックで確認されたポアの数より、シークエンシング開始時のポア数が少なく表示された。 | フローセルがデバイスに正しく挿入されていない。 | シークエンスランを停止し、フローセルをシークエンス装置から取り出します。次に再度フローセルを挿入し、装置にしっかりと固定され、目標温度に達していることを確認します。GridIONやPromethIONの場合は別のフローセルの位置をお試しください。 |
| MinKNOWのフローセルチェックで確認されたポアの数より、シークエンシング開始時のポア数が少なく表示された。 | ライブラリー内の汚染物質がポアを失活させたり塞いだりしている。 | フローセルチェックの際のポア数は、フローセル保存バッファー中のQC用のDNA分子を用いて計測されます。シークエンシングの開始時は、ライブラリ自体を使用してアクティブなポア数を推定します。このため、フローセルチェックとRun開始時のポア数は、約10%程度の変動が起こります。シークエンシング開始時に報告されたポアの数が大幅に減少している場合は、ライブラリー中の汚染物質がメンブレンを損傷していたり、ポアをブロックしている可能性があります。インプット材料の純度を向上させるために、別のDNA/RNA抽出または精製方法が必要となる場合があります。コンタミネーションの影響は、Contaminants Know-how pieceを参照にして下さい。夾雑物を除去するために別の抽出方法extraction method をお試しください。 |
MinKNOWのスクリプトに問題
| 問題点 | この問題が生じた可能性のある原因 | 解決策とコメント |
|---|---|---|
| MinKNOW に 「Script failed」と表示されている" | コンピューターを再起動し、MinKNOWを再起動します。問題が解決しない場合は MinKNOW log files MinKNOWログファイルを収集し 、テクニカルサポートにご連絡ください。他のシークエンシングデバイスをお持ちでない場合は、 フローセルとロードしたライブラリーを4℃で保管することをお勧めします。詳細な保管方法については、テクニカルサポートにお問い合わせください。 |
ポア占有率が40%未満
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| ポアの占有率が40%以下 | フローセルに十分なライブラリーがロードされていなかった。 | シークエンシングライブラリーを正確に濃度測定し、適切な容量がフローセルにロードされていることを確認してください(詳しくはそれぞれのプロトコールをご覧ください)。 ロードする前にライブラリーを定量し、 Promega Biomath Calculatorなどのツールを使用してfmolを計算してください。[dsDNA: µ g to fmol]を選択してください。 |
| ポア占有率が0に近い | Ligation Sequencing Kitを使用したが、シークエンシングアダプターはDNAにライゲーションしなかった。 | シークエンシングアダプターのライゲーションステップでは、必ずNEBNext Quick Ligation Module(E6056)とOxford Nanopore Technologies Ligation Buffer(LNB、シークエンスキットに付属されています。)を使用し、各試薬の量を適切に使用してください。サードパーティ試薬の完全性をテストするために、Lambdaのコントロールライブラリーを調製することもできます。 |
| ポア占有率が0に近い | シークエンシングアダプターライゲーション後の洗浄工程で、LFBまたはSFBの代わりにエタノールを使用してしまった。 | エタノールはシークエンシングアダプター上のモータータンパク質を変性させる可能性があります。シークエンシングアダプターのライゲーション後にLFBまたはSFBバッファーを使用したことを確認して下さい。 |
| ポア占有率が0に近い | フローセルにテザーがない | テザーはフローセルのプライミング時に追加されます(キット9、10、11はFLTチューブ、キット14はFTUを使用。ウルトラロングのDNAキットにはFTUを使用。) プライミングの前に、FLT/FCT/FTUがバッファー(キット9、10、11はFB、キット14はFCF)に添加されていることを確認してください。 |
予想より短いリード長
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| 予想より短いリード長 | DNAサンプルの不要な断片化 | 読み取り長はサンプルDNA断片の長さを反映します。サンプルDNAは、抽出およびライブラリー調製中の操作で断片化した可能性があります。 1. 抽出の最適な方法については、Extraction Methods の抽出方法を参照してください。 2. ライブラリー調製に進む前に、アガロースゲル電気泳動で、サンプルDNAのフラグメント長の分布を確認してください。 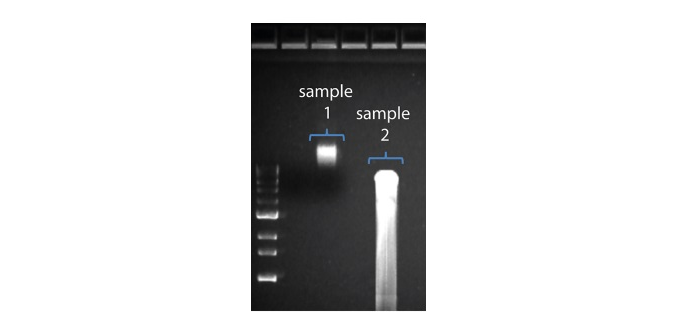 上の画像では、サンプル1は高分子量ですが、サンプル2は断片化されています。 上の画像では、サンプル1は高分子量ですが、サンプル2は断片化されています。3. ライブラリー調製中は、試薬を混合するためのピペッティングやボルテックス操作は、プロトコルで指示がないかぎり行わないでください。 |
利用できないポアの割合が多い場合
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
利用できないポアの割合が大きい(チャンネルパネルとポアのアクティブポートで青く表示されています) 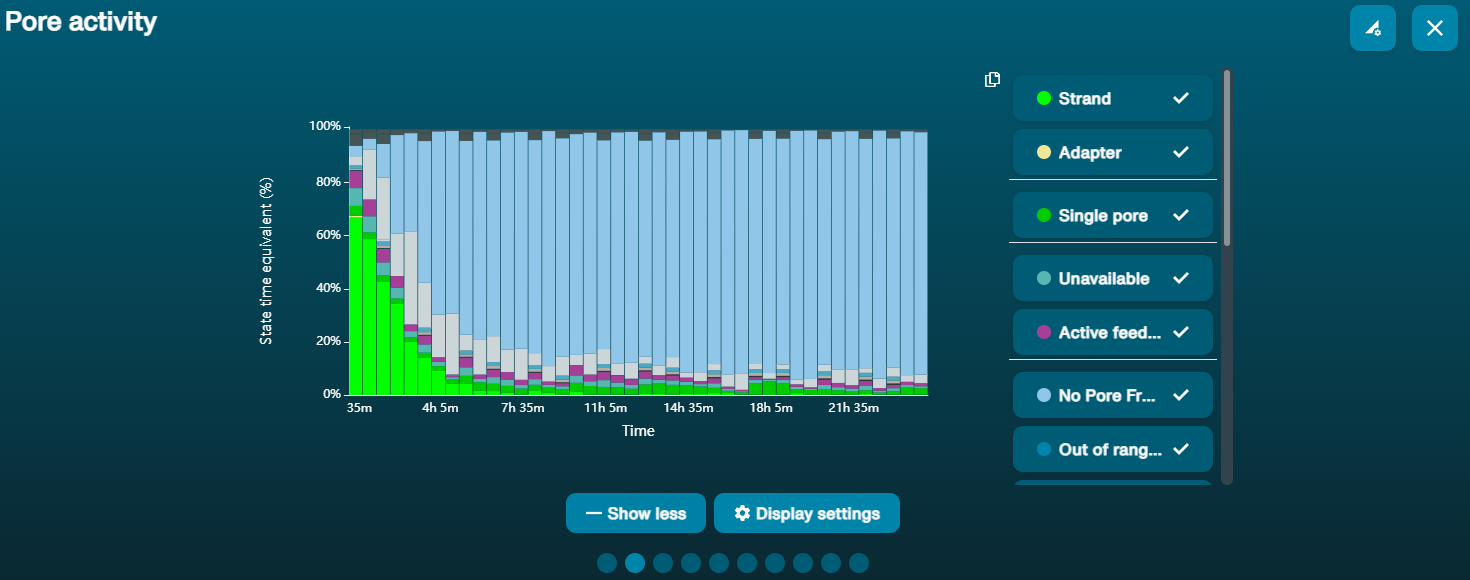 上のアクティブなポアの図は、時間の経過とともに「利用できない」ポアの割合が増加していることを示しています。 上のアクティブなポアの図は、時間の経過とともに「利用できない」ポアの割合が増加していることを示しています。 | サンプル内に不純物が含まれている | 一部のポアに吸着する不純物は、MinKNOWに組み込まれたポアのブロック解除機能によって、ポアから除去することができます。 このステップが完了すると、ポアの状態が「sequencing pore」に戻ります。利用できないポアの部分が多いか、増加した場合: 1.Flow Cell Wash Kit nuclease flush using the Flow Cell Wash Kit (EXP-WSH004) を用いて、ヌクレアーゼ洗浄を 行うことができます。又は 2. PCRを数サイクル実行してサンプルDNAの量を増やし、サンプルDNAに含まれる問題の不純物が相対的に減る(希釈される)ようにします。 |
Inactiveのポアの割合が高い
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| 利用できない(inactive/unavailable)ポアの割合が高い(チャネルパネルとポアアクティブポートでは水色で表示されています)ポアまたは膜に損傷が起きてしまった。 | 気泡がフローセルに混入した。 | フローセルのプライミングやライブラリーのロードで気泡が入ると、ポアに不可逆的なダメージを与える可能性があります。 推奨の操作方法については、Priming and loading your flow cell のビデオをご覧ください。 |
| 利用できないポアの割合が多い場合 | サンプルDNAに含まれる不純物 | 既知の化合物問題で、サンプルDNAに多糖類が含まれた事で、植物のゲノムDNAと結合しポアをブロックした。 1. 植物葉DNA抽出法 Plant leaf DNA extraction methodをご参照ください。 2. QIAGEN PowerClean Pro キットを使用してクリーンアップして下さい。 3. QIAGEN REPLI-g kit.キットを使用して、元のgDNAサンプルで全ゲノム増幅を実行します。 |
| 利用できないポアの割合が多い場合 | サンプル内に不純物が含まれている | 不純物の影響は、 Contaminants の ノウハウを参照して下さい。 サンプルDNAに不純物を残留させないために別の抽出方法をお試しください。 |
温度変動
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| 温度変動 | フローセルとデバイスの接続が途切れている。 | フローセルの背面にある金属プレートを覆っているヒートパッドがあることを確認してください。 フローセルを再度挿入し、コネクターピンがデバイスにしっかりと接触していることを確認するために軽く押してください。問題が解決しない場合は、テクニカルサービスにご連絡してください。 |
目標温度に到達しない場合
| 問題点 | 予想される原因 | 解決策とコメント |
|---|---|---|
| MinKNOWが "Failed to reach target temperature "(目標温度に達しなかった)と表示する。" | 装置が通常の室温より低い場所、または風通しの悪い場所(排気が出来ない場所)に置かれた時にフローセルが過熱してします。 | MinKNOWでは、フローセルが目標温度に到達するまでの既定の時間枠があります。時間枠を超えると、エラーメッセージが表示され、シークエンシング実験が続行されます。しかし、不適切な温度でシークエンスを行うと、スループットが低下し、qスコアが低下する可能性があります。シークエンシングデバイスが風通しの良い室温に置かれていることを確認して、MinKNOW再スタートしてください。MinION Mk 1Bの温度制御の詳細については、FAQ を参照してください。 |







