Secuenciación transcriptómica de células individuales a partir de ADNc 5′ preparado con 10x Genomics y el kit SQK-LSK114 (SST_9204_v114_revM_26Sep2025)
PromethION: Protocol
Secuenciación transcriptómica de células individuales a partir de ADNc 5′ preparado con 10x Genomics y el kit SQK-LSK114 V SST_9204_v114_revM_26Sep2025
Método de secuenciación transciptómica de células individuales:
Este protocolo:
- Requiere amplicones de ADNc generados con los ensayos Chromium GEM-X Universal 5’ Gene Expression (V3) o Chromium Next GEM Universal 5’ Gene Expression (V2) de 10x Genomics.
- La preparación de la biblioteca dura aproximadamente 140 minutos.
- Genera gran cantidad de datos.
- Incluye PCR.
De uso exclusivo en investigación
FOR RESEARCH USE ONLY.
Contents
Introducción al protocolo
Preparación de la biblioteca
- 3. Amplificación por PCR
- 4. Preparación de extremos
- 5. Ligación de los adaptadores y purificación
- 6. Acondicionamiento y carga de celdas de flujo PromethION
Secuenciación y análisis de datos
- 7. Adquisición de datos e identificación de bases
- 8. Reutilización y devolución de celdas de flujo
- 9. Análisis de datos
Resolución de problemas
Descripción general
Método de secuenciación transciptómica de células individuales:
Este protocolo:
- Requiere amplicones de ADNc generados con los ensayos Chromium GEM-X Universal 5’ Gene Expression (V3) o Chromium Next GEM Universal 5’ Gene Expression (V2) de 10x Genomics.
- La preparación de la biblioteca dura aproximadamente 140 minutos.
- Genera gran cantidad de datos.
- Incluye PCR.
De uso exclusivo en investigación
1. Descripción general
Introducción al protocolo de transcriptómica 5’ de células individuales
Esta aplicación secuencia transcritos de ADNc completos en el extremo 5’, lo que ofrece una visión integral de las isoformas expresadas y facilita la identificación de eventos de empalme alternativo y fusiones en células individuales. Además, detecta SNP en cualquier parte del transcrito e identifica subtipos celulares dentro de una población a partir de los niveles de expresión de las isoformas.
Este protocolo describe cómo llevar a cabo la secuenciación de ADNc a partir de células individuales mediante el kit de secuenciación Ligation Sequencing Kit V14 (SQK-LSK114). Deberá haber retrotranscrito el ARNm de células individuales en ADNc con los ensayos Chromium GEM-X Universal 5' Gene Expression (V3) o Chromium Next GEM Universal 5' Gene Expression (V2) de 10x Genomics, antes de amplificar el ADNc por PCR con oligonucleótidos personalizados. Por último, se realiza una preparación normal de la biblioteca con el kit Ligation Sequencing Kit V14, con la que se acondicionan los extremos de ADNc antes de secuenciar en un dispositivo PromethION.
Este protocolo está optimizado y adaptado para utilizarse con el protocolo Secuenciación transcriptómica de células individuales a partir de ADNc 3′ preparado con 10x Genomics, el kit SQK-LSK114 y la ampliación EXP-PCA001.
El protocolo original de 3' se adaptó a partir de Lebrigand, K., Magnone, V., Barbry, P. et al. High throughput error‑corrected Nanopore single‑cell transcriptome sequencing. Nature Communications 11, 4025 (2020), con el fin de secuenciar transcritos de longitud completa, eliminar artefactos de la síntesis de ADNc y corregir el sesgo de hebra.
Importante: este protocolo se ha elaborado para utilizarse con los ensayos Chromium GEM-X Universal 5' Gene Expression (V3) o Chromium Next GEM Universal 5' Gene Expression (V2) de 10x Genomics.
Si trabaja con los ensayos Chromium GEM-X Universal 3’ Gene Expression (V4) o Chromium Next GEM Universal 3’ Gene Expression (V3.1) de 10x Genomics, consulte el protocolo Secuenciación transcriptómica de células individuales a partir de ADNc 3′ preparado con 10x Genomics y los kits SQK-LSK114 y EXP-PCA001.
Si utiliza los ensayos Visium Spatial Gene Expression (Visium V1 para muestras congeladas en fresco) o Visium HD 3' Spatial Gene Expression, consulte el protocolo Spatial transcriptomics sequencing from 3’ cDNA prepared with 10x Genomics using SQK-LSK114 and EXP-PCA001.
Pasos del proceso de secuenciación:
Preparación del experimento
Pasos:
- Preparar con anterioridad el ADNc de células individuales, con los ensayos Chromium GEM-X Universal 5' Gene Expression (V3) o Chromium Next GEM Universal 5' Gene Expression (V2) de 10x Genomics. Este método requiere utilizar una muestra de buena calidad. Además, los controles de calidad realizados durante el protocolo son esenciales para garantizar el éxito del experimento.
- Tener a disposición el kit de secuenciación, el instrumental pertinente y los reactivos de otros fabricantes.
- Descargar el programa MinKNOW que obtiene y analiza los datos.
- Verificar la(s) celda(s) de flujo y comprobar que tiene(n) poros suficientes para realizar una buena secuenciación.
Preparación de la biblioteca
| Pasos | Procedimiento | Duración | Parada opcional |
|---|---|---|---|
| Amplificación por PCR | Amplificar el ADNc por PCR | 80 min | - |
| Preparación de extremos | Preparar los extremos de ADNc antes de ligar los adaptadores | 30 minutos | 4 °C hasta el día siguiente |
| Ligación de los adaptadores y purificación | Ligar los adaptadores al ADNc | 20 min | 4 °C durante almacenamientos breves o en caso de uso repetido, como la recarga de celdas de flujo. –80 °C durante almacenamientos prolongados. |
| Acondicionar y cargar la celda de flujo | Acondicionar la celda de flujo y cargar la biblioteca preparada | 10 minutos |
Secuenciación y análisis
Pasos:
- Empezar el proceso de secuenciación desde el programa MinKNOW, que obtendrá datos brutos del dispositivo e identificará las lecturas.
- Analizar los datos con el flujo bioinformático wf-single-cell de EPI2ME.
Compatibilidad del protocolo
Este protocolo debería usarse solo en combinación con los siguientes productos:
- Kit Ligation Sequencing V14 (SQK-LSK114)
- Celdas de flujo R10.4.1 (FLO-PRO114M)
- Kit Flow Cell Wash (EXP-WSH004)
- Dispositivo PromethION - PromethION IT Requirements document
2. Material y consumibles
Material
- 10 ng de amplicones de ADNc producidos con los ensayos Chromium GEM-X Universal 5’ Gene Expression (V3) o Chromium Next GEM Universal 5’ Gene Expression (V2)
- Oligo de encargo a 10 μM: Fwd_3580_partial_read1_defined_for_5'_cDNA (secuencia indicada a continuación)
- Oligo de encargo a 10 μM: Rev_PR2_partial_TSO_defined_for_5'_cDNA (secuencia indicada a continuación)
- Kit Ligation Sequencing V14 (SQK-LSK114)
Consumibles
- Celdas de flujo PromethION (FLO-PRO114M)
- Mezcla maestra 2X LongAmp Hot Start Taq (NEB, M0533)
- Módulo NEBNext® Ultra™ II End Repair/dA-Tailing (NEB, E7546)
- Ligasa de ADN Salt-T4® (NEB, M0467)
- Kit Qubit 1x dsDNA HS (ThermoFisher, Q33230)
- Kit Agilent Technologies DNA 12000
- Microesferas Agencourt AMPure XP (Beckman Coulter™, A63881)
- Etanol al 80 % recién preparado con agua sin nucleasas
- Agua sin nucleasas (p.ej. Thermo Scientific, AM9937)
- Tubos Falcon de 15 ml
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Tubos de PCR de pared fina, 0,2 ml
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Pantalla protectora celdas de flujo PromethION
- Dispositivo PromethION
- Bioanalizador Agilent (o equivalente)
- Hula mixer (mezclador de rotación suave)
- Gradilla magnética (p. ej., Invitrogen DynaMag-2 Magnet, 12321D)
- Microcentrífuga
- Mezclador vórtex
- Termociclador
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P100
- Pipeta y puntas P20
- Pipeta y puntas P10
- Pipeta y puntas P2
- Cubeta con hielo
- Temporizador
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
En este protocolo, se necesitan 10 ng de amplicones de ADNc amplificados, preparados con uno de los ensayos de 10x Genomics: Chromium GEM-X Universal 5' Gene Expression (V3) o Chromium Next GEM Universal 5' Gene Expression (V2).
Kits de 10x Genomics
Importante: este protocolo debe utilizarse con los ensayos Chromium GEM-X Universal 5' Gene Expression (V3) o Chromium Next GEM Universal 5' Gene Expression (V2) de 10x Genomics.
El protocolo Secuenciación transcriptómica de células individuales a partir de ADNc 3′ preparado con 10x Genomics y los kits SQK-LSK114 y EXP-PCA001 debe utilizarse con uno de los ensayos de 10x Genomics: Chromium GEM-X Universal 3’ Gene Expression (V4) o Chromium Next GEM Universal 3’ Gene Expression (V3.1).
Si utiliza uno de los ensayos de 10x Genomics, Visium Spatial Gene Expression (Visium V1 para muestras congeladas en fresco) o Visium HD 3' Spatial Gene Expression, consulte el protocolo Spatial transcriptomics sequencing from 3’ cDNA prepared with 10x Genomics using SQK-LSK114 and EXP-PCA001.
Secuencias de oligonucleótidos personalizadas
Pida los siguientes oligonucleótidos purificados por HPLC a una concentración de 100 μM y dilúyalos a 10 μM en amortiguador TE, que utilizará en el paso de amplificación por PCR de la preparación de la biblioteca.
| Nombre | Secuencia |
|---|---|
| Fwd_3580_partial_read1_defined_for_5'_cDNA | 5'-/5phos/ACTTGCCTGTCGC TCTATCTTCCTACACGA CGCTCTTCCGATCT-3' |
| Rev_PR2_partial_TSO_defined_for_5'_cDNA | 5'-/5phos/TTTCTGTTGGTGC TGATATTGCAAGCAGTG GTATCAACGCAGAG-3' |
Microesferas AMPure XP
En los primeros pasos, cuando se preparen los amplicones de ADNc se necesitará una cantidad adicional de microesferas AMPure XP. A partir de la preparación de extremos, es posible utilizar las microesferas AMPure XP del kit de secuenciación por ligación V14 (SQK-LSK114).
Muestra de ADN
Verificar la calidad de la muestra inicial de ADN
Es importante que la muestra de ADN cumpla con los requisitos de cantidad y calidad. Usar demasiado ADN, poco o de mala calidad (p. ej., que esté muy fragmentado, que contenga ARN o contaminantes químicos), en ocasiones afecta a la preparación de la biblioteca.
Siga las instrucciones sobre cómo realizar un control de calidad de la muestra de ADN, en el protocolo Input DNA/ RNA QC.
Contaminantes químicos
Según cómo se extraiga el ADN de la muestra original, ciertos contaminantes químicos quedan en el ADN purificado y afectan tanto a la eficacia de la preparación de la biblioteca como a la calidad de la secuenciación. Encontrará más información sobre contaminantes en la página Contaminants de la comunidad Nanopore.
Reactivos de otros fabricantes
Hemos probado y recomendamos el uso de todos los reactivos de otros fabricantes usados en este protocolo. Oxford Nanopore Technologies no ha evaluado otras alternativas.
Recomendamos preparar estos reactivos siguiendo las instrucciones del fabricante.
Evaluación de la celda de flujo
Antes de empezar el experimento de secuenciación, recomendamos comprobar el número de poros disponibles presentes en la celda de flujo. La comprobación debe realizarse en un plazo de 12 semanas desde la compra. Oxford Nanopore Technologies sustituirá cualquier celda de flujo con un número de poros inferior al indicado en la tabla siguiente, siempre y cuando el resultado se notifique dentro de los dos días siguientes a la evaluación y se hayan seguido las instrucciones de almacenamiento. Encontrará más información en las instrucciones del documento Flow Cell Check.
| Celdas de flujo | Cantidad mínima de poros activos cubierta por la garantía |
|---|---|
| PromethION | 5 000 |
Contenido del kit Ligation Sequencing Kit V14 (SQK-LSK114)
Nota: este producto contiene un reactivo, AMPure XP, fabricado por Beckman Coulter Inc., y el almacenamiento a –20 °C, junto con el kit, no perjudica su estabilidad.
Nota: DNA Control Sample (DCS) es un amplicón estándar de 3,6 kb que se alinea con el extremo 3’ del genoma Lambda.
3. Amplificación por PCR
Material
- 10 ng de amplicones de ADNc producidos con los ensayos Chromium GEM-X Universal 5’ Gene Expression (V3) o Chromium Next GEM Universal 5’ Gene Expression (V2)
- Oligo de encargo a 10 μM: Fwd_3580_partial_read1_defined_for_5'_cDNA (secuencia proporcionada en la sección anterior)
- Oligo de encargo a 10 μM: Rev_PR2_partial_TSO_defined_for_5'_cDNA (secuencia proporcionada en la sección anterior)
Consumibles
- Mezcla maestra 2X LongAmp Hot Start Taq (NEB, M0533)
- Microesferas Agencourt AMPure XP (Beckman Coulter™, A63881)
- Kit Qubit 1x dsDNA HS (ThermoFisher, Q33230)
- Kit Agilent Technologies DNA 12000
- Etanol al 80 % recién preparado con agua sin nucleasas
- Agua sin nucleasas (p. ej., ThermoFisher, AM9937)
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Tubos de PCR de pared fina, 0,2 ml
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Termociclador
- Microcentrífuga
- Hula mixer (mezclador de rotación suave)
- Gradilla magnética (p. ej., Invitrogen DynaMag-2 Magnet, 12321D)
- Cubeta con hielo
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P100
- Pipeta y puntas P20
- Pipeta y puntas P2
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
Equipo opcional
- Bioanalizador Agilent (o equivalente)
Comprobación de la celda de flujo.
Recomendamos verificar la celda de flujo antes de empezar a preparar la biblioteca, y así comprobar que tenga poros suficientes para realizar una buena secuenciación.
Encontrará más información en el documento Flow cell check.
Preparar los amplicones de ADNc en agua sin nucleasas:
- Transferir 10 ng de amplicones de ADNc a un tubo de PCR de pared fina (0,2 ml).
- Ajustar el volumen a un total de 21 µl con agua sin nucleasas.
- Mezclar golpeando suavemente el tubo con el dedo para evitar fragmentaciones indeseadas.
- Centrifugar brevemente en una microcentrífuga.
En el mismo tubo de PCR de pared fina (0,2 ml), preparar la siguiente reacción:
| Reactivo | Solución madre | Concentración final | Volumen |
|---|---|---|---|
| Molde de ADNc | 0,48 ng/μl | 0,2 ng/μl | 21 μl |
| [Btn]Fwd_3580_partial_read1_defined_for_5'_ADNc | 10 μM | 0,4 μM | 2 μl |
| Rev_PR2_partial_TSO_defined_for_5'_ADNc | 10 μM | 0,4 μM | 2 μl |
| Mezcla maestra LongAmp Hot Start Taq 2X | 2× | 1× | 25 μl |
| Total | - | - | 50 μl |
Mezclar con la pipeta y centrifugar brevemente.
Amplificar mediante las siguientes condiciones de ciclado:
| Paso | Temperatura | Velocidad de cambio | Duración | N.º de ciclos |
|---|---|---|---|---|
| Desnaturalización inicial | 94 °C | máx. | 3 min | 1 |
| Desnaturalización Descenso hacia la temperatura de hibridación Hibridación Extensión | 94 °C de 66 °C a 58 °C 58 °C 65 °C | max 0.2 °C/s máx. máx. | 30 s 40 s 50 s 6 min | 8 |
| Extensión final | 65 °C | max | 10 min | 1 |
| Mantenimiento | 4 °C | - | ∞ | - |
El siguiente esquema muestra las etapas y condiciones térmicas del ciclado. 
Transferir la muestra a un tubo nuevo de 1,5 ml Eppendorf DNA Lobind.
Resuspender las microesferas AMPure XP mediante vórtex.
Añadir 40 μl de microesferas resuspendidas AMPure XP a la mezcla de reacción y dar suaves golpes al tubo con el dedo.
Incubar en el hula mixer (o mezclador rotatorio) durante 5 minutos a temperatura ambiente.
Preparar 500 µl de etanol al 80 % con agua sin nucleasas.
Centrifugar las muestras y separar las microesferas en una gradilla magnética hasta que el eluido se vuelva claro e incoloro. Sin mover el tubo, retirar el sobrenadante con una pipeta.
Mantener el tubo en la gradilla magnética, lavar las microesferas con 200 µl de etanol al 80 % recién preparado en agua sin nucleasas, sin desplazar el sedimento. Retirar el etanol con una pipeta y desechar.
Repetir el paso anterior.
Centrifugar brevemente y colocar el tubo de nuevo en la gradilla magnética. Retirar con una pipeta cualquier residuo de etanol. Dejar secar el sedimento durante 30 s aproximadamente, sin dejar que se agriete.
Quitar el tubo de la gradilla magnética y resuspender el sedimento en 15 µl de agua sin nucleasas. Centrifugar e incubar durante 2 min a temperatura ambiente.
Separar las microesferas en una gradilla magnética, durante al menos 1 minuto, hasta que el eluido se vuelva claro e incoloro.
Extraer y guardar 15 µl de eluido en un tubo nuevo Eppendorf DNA Lobind de 1,5 ml.
Deshechar las microesferas sedimentadas.
Cuantificar 1 μl de muestra eluida con un fluorímetro Qubit - se espera recuperar una cantidad superior a 100 ng.
Cuantificar 200 fmol de ADNc a partir del tamaño medio de fragmento, identificado con un Bioanalyzer de Agilent.
En su defecto, se asume un tamaño medio de fragmento de 1kbp.
Figura: ejemplo de distribución de longitudes de fragmento de amplicones: tres reproducciones biológicas de ADNc 5' de PBMCs, preparado con el ensayo Chromium Next GEM Universal 5’ Gene Expression (V2) de 10x Genomics y procesadas con el protocolo de ADNc 5’ 10x de Oxford Nanopore Technologies. En este caso, los amplicones se han analizado con el Bioanalyzer 2100 y el kit DNA 12000.
Transferir 200 fmol de ADNc al paso de preparación de extremos.
4. Preparación de extremos
Material
- 200 fmol de amplicones de ADNc
- AMPure XP Beads (AXP)
Consumibles
- Mezcla enzimática NEBNext® Ultra II End Prep, del módulo NEBNext® Ultra II End Repair (NEB, E7546)
- Amortiguador de reacción NEBNext® Ultra II End Prep, del módulo NEBNext® Ultra II End Repair (NEB, E7546)
- Kit Qubit dsDNA HS (Invitrogen Q32851)
- Agua sin nucleasas (p.ej. Thermo Scientific, AM9937)
- Etanol al 80 % recién preparado con agua sin nucleasas
- Tubos de PCR de pared fina, 0,2 ml
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Pipeta y puntas P1000
- Pipeta y puntas P100
- Pipeta y puntas P10
- Termociclador
- Microcentrífuga
- Hula mixer (mezclador de rotación suave)
- Gradilla magnética
- Cubeta con hielo
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
Preparar los reactivos NEBNext Ultra II End Repair/dA-tailing Module de acuerdo con las instrucciones del fabricante y poner en hielo:
A fin de obtener un rendimiento óptimo, NEB recomienda lo siguiente:
Descongelar los reactivos en hielo.
Mezclar el contenido de todos los tubos.
Nota: no mezclar en vórtex la mezcla Ultra II End Prep Enzyme Mix.
Centrifugar brevemente los tubos antes de abrirlos.
El reactivo NEBNext Ultra II End Prep Reaction Buffer tal vez contenga un precipitado blanco. En tal caso, dejar que la mezcla alcance la temperatura ambiente y pipetear el amortiguador varias veces hasta dispersar el precipitado. Después, agitar brevemente en vórtex.
Transferir 200 fmol de amplicón de ADNc en un tubo nuevo de PCR —de pared fina y 0,2 ml— y ajustar el volumen a 50 µl con agua sin nucleasas.
En el mismo tubo de PCR, mezclar lo siguiente:
Entre cada adición, mezclar con la pipeta de 10 a 20 veces.
| Reactivo | Volumen |
|---|---|
| Amplicones de ADNc | 50 µl |
| Ultra II End-prep Reaction Buffer | 7 µl |
| Ultra II End-prep Enzyme Mix | 3 µl |
| Total | 60 µl |
Mezclar bien la reacción con la pipeta y centrifugar brevemente.
Incubar en el termociclador, a 20 ºC durante 5 min y a 65 ºC durante 5 min. Mantener a 4 ºC.
Transferir la muestra de ADN a un tubo nuevo Eppendorf DNA Lobind de 1,5 ml.
Resuspender las microesferas AMPure XP (AXP) mediante vórtex.
Añadir 60 µl de microesferas AMPure XP Beads (AXP) resuspendidas a la mezcla de preparación de extremos y mezclar golpeando suavemente el tubo con el dedo.
Incubar en el hula mixer (o mezclador rotatorio) durante 5 minutos a temperatura ambiente.
Preparar 500 µl de etanol al 80 % con agua sin nucleasas.
Centrifugar brevemente la muestra y sedimentar en una gradilla magnética hasta que el sobrenadante se vuelva claro e incoloro. Sin mover el tubo, retirarlo con una pipeta y desechar.
Sin mover el tubo, lavar las microesferas con 200 µl de etanol al 80 %, sin desplazar el sedimento. Retirar el etanol con una pipeta y desechar.
Repetir el paso anterior.
Centrifugar brevemente y colocar el tubo de nuevo en la gradilla magnética. Retirar con una pipeta cualquier residuo de etanol. Dejar secar el sedimento durante 30 s aproximadamente, sin dejar que se agriete.
Quitar el tubo de la gradilla magnética y resuspender el sedimento en 61 µl de agua sin nucleasas dando suaves golpes al tubo con el dedo. Incubar durante 2 minutos a temperatura ambiente.
Sedimentar las microesferas en una gradilla magnética, durante al menos 1 minuto, hasta que el eluido se vuelva claro e incoloro.
Extraer y guardar 61 µl de eluido en un tubo nuevo Eppendorf DNA Lobind de 1,5 ml.
Cuantificar 1 μl de muestra eluida con un fluorímetro Qubit.
Tomar el ADN reparado y proceder a la ligación de los adaptadores. En este paso, también se puede guardar la muestra a 4 °C hasta el día siguiente.
5. Ligación de los adaptadores y purificación
Material
- Ligation Adapter (LA)
- Ligation Buffer (LNB)
- Short Fragment Buffer (SFB)
- AMPure XP Beads (AXP)
- Elution Buffer (EB)
Consumibles
- Kit Qubit dsDNA HS (Invitrogen Q32851)
- Ligasa de ADN Salt-T4® (NEB, M0467)
- Tubos Eppendorf DNA LoBind de 1,5 ml
- Tubos Qubit™ Assay (Invitrogen, Q32856)
Instrumental
- Gradilla magnética
- Hula mixer (rotator mixer)
- Microcentrífuga
- Mezclador vórtex
- Pipeta y puntas P1000
- Pipeta y puntas P100
- Pipeta y puntas P20
- Pipeta y puntas P10
- Fluorímetro Qubit™ (o equivalente para el control de calidad)
Recomendamos utilizar la ligasa de ADN Salt-T4®(NEB, M0467).
Se adquiere por separado o con el módulo NEBNext® Companion v2 de secuenciación por ligación de Oxford Nanopore Technologies® (NEB E7672S o E7672L).
La ligasa de ADN Quick T4 (NEB E6057) incluida en la versión anterior del módulo NEBNext® Companion Module de Oxford Nanopore Technologies® (NEB E7180S or E7180L) también es compatible, pero el nuevo reactivo recomendado ofrece una ligación más eficiente.
Aunque las ligasas recomendadas de otros fabricantes incluyan su propio amortiguador, la eficiencia del adaptador —Ligation Adapter (LA)—, es mayor cuando se usa el amortiguador Ligation Buffer (LNB) incluido en el kit Ligation Sequencing Kit.
Centrifugar los viales Ligation Adapter (LA) y Salt-T4® DNA Ligase y poner en hielo.
Descongelar el vial Ligation Buffer (LNB) a temperatura ambiente, centrifugar y mezclar con la pipeta. Debido a su viscosidad, la agitación en vórtex de este amortiguador es ineficaz. Tras descongelar y mezclar, colocar en hielo de inmediato.
Descongelar el vial Elution Buffer (EB) a temperatura ambiente y mezclar en vórtex. Centrifugar brevemente y poner en hielo.
Descongelar el reactivo Long Fragment Buffer (SFB) a temperatura ambiente y mezclar en vórtex. Centrifugar brevemente y poner en hielo.
En un tubo Eppendorf DNA LoBind de 1,5 ml, mezclar en el siguiente orden:
Entre cada adición, mezclar con la pipeta de 10 a 20 veces.
| Reactivo | Volumen |
|---|---|
| Muestra de ADN del paso anterior | 60 µl |
| Ligation Adapter (LA) | 5 µl |
| Ligation Buffer (LNB) | 25 µl |
| Salt-T4® DNA Ligase | 10 µl |
| Total | 100 µl |
Mezclar bien la reacción con la pipeta y centrifugar brevemente.
Incubar la reacción durante 10 minutos a temperatura ambiente.
Resuspender las microesferas AMPure XP (AXP) mediante vórtex.
Añadir 40 μl de microesferas AMPure XP Beads (AXP) resuspendidas a la mezcla de reacción y dar suaves golpes al tubo con el dedo.
Incubar en el hula mixer (o mezclador rotatorio) durante 5 minutos a temperatura ambiente.
Centrifugar brevemente la muestra y sedimentar en una gradilla magnética. Esperar hasta que el sobrenadante se aclare y retirar con la pipeta.
Lavar las microesferas con 250 μl de Short Fragment Buffer (SFB). Golpear el tubo suavemente con el dedo, centrifugar brevemente, colocar de nuevo en la gradilla magnética y dejar que las microesferas sedimenten. Retirar el sobrenadante con una pipeta y desechar.
Nota: retirar el sobrenadante con cuidado; la viscosidad del amortiguador tal vez contribuya a perder microesferas del precipitado.
Repetir el paso anterior.
Centrifugar brevemente y colocar el tubo de nuevo en la gradilla magnética. Retirar con una pipeta el resto del sobrenadante. Dejar secar el sedimento durante 30 s aproximadamente, sin dejar que se agriete.
Quitar el tubo de la gradilla magnética y resuspender el sedimento en 34 µl de Elution Buffer (EB).
Centrifugar la muestra e incubar durante 10 minutos a temperatura ambiente.
Nota: con ADN de elevado peso molecular, la incubación a 37 °C mejora la recuperación de fragmentos largos.
Sedimentar las microesferas en una gradilla magnética, durante al menos 1 minuto, hasta que el eluido se aclare.
Extraer y conservar 34 μl del eluido que contiene la biblioteca de ADN en un tubo nuevo Eppendorf DNA LoBind de 1,5 ml.
Cuantificar 1 μl de muestra eluida con un fluorímetro Qubit.
Diluir entre 50 y 100 fmol de biblioteca preparada en 32 μl de Elution Buffer (EB).
En su defecto, asumir una longitud media de fragmento de 1 kbp y continuar con 33 ng de biblioteca.
Nota: si la biblioteca de ADN está por debajo de la concentración requerida, utilice el volumen completo —32 μl de ADN eluido— en la secuenciación.
Atención: tenga en cuenta que una recuperación muy baja tal vez se deba a un fallo en la preparación de la biblioteca.
Si se necesita calculadora, recomendamos utilizar una de masa a moles como la calculadora de NEB.
Recomendamos cargar entre 50 y 100 fmol de esta última biblioteca, en la celda de flujo R10.4.1.
Cargar la concentración recomendada garantizará una ocupación de poros óptima y un elevado rendimiento de secuenciación. Si es necesario, diluir la biblioteca en Elution Buffer (EB).
La biblioteca preparada se cargará en la celda de flujo. Conservar la biblioteca en hielo o a 4 °C hasta el momento de cargar.
Recomendaciones de almacenamiento
Recomendamos guardar las bibliotecas en tubos Eppendorf DNA LoBind a 4 °C, durante periodos de tiempo cortos o en caso de uso repetido, por ejemplo, para recargar celdas de flujo entre lavados. Para uso individual y conservar a largo plazo durante periodos de más de 3 meses, recomendamos guardar las bibliotecas a –80 °C en tubos Eppendorf DNA LoBind.
6. Acondicionamiento y carga de celdas de flujo PromethION
Material
- Sequencing Buffer (SB)
- Library Beads (LIB)
- Library Solution (LIS)
- Flow Cell Tether (FCT)
- Flow Cell Flush (FCF)
Consumibles
- Celdas de flujo PromethION
- Tubos Eppendorf DNA LoBind de 1,5 ml
Instrumental
- Dispositivo PromethION
- Pantalla protectora celdas de flujo PromethION
- Pipeta y puntas P1000
- Pipeta y puntas P200
- Pipeta y puntas P20
Este kit es compatible solo con celdas de flujo R10.4.1 (FLO-PRO114M).
Tras sacar la(s) celda(s) de flujo de la nevera, esperar 20 minutos a que alcance(n) la temperatura ambiente antes de insertarla(s) en el PromethION. En ambientes húmedos puede formarse condensación. Inspeccione las clavijas doradas del conector, situadas en la parte superior e inferior, en busca de condensación y si la hubiera, límpiela con una toallita sin pelusa. Compruebe que haya una almohadilla térmica negra pegada en la parte posterior.
Descongelar los viales Sequencing Buffer (SB), Library Beads (LIB) o Library Solution (LIS), —si se necesita—, Flow Cell Tether (FCT) y un tubo de Flow Cell Flush (FCF) a temperatura ambiente y mezclar en vórtex. Centrifugar brevemente y poner en hielo.
Preparar la mezcla de acondiciomiento; para ello, combinar Flow Cell Tether (FCT) y Flow Cell Flush (FCF) como se indica a continuación. Agitar en vórtex a temperatura ambiente.
En un tubo proporcionado al número de celdas de flujo que se vayan a utilizar, combinar los siguientes reactivos:
| Reactivo | Volumen por celda de flujo |
|---|---|
| Flow Cell Flush (FCF) | 1 170 µl |
| Flow Cell Tether (FCT) | 30 µl |
| Total volume | 1 200 µl |
Cargar la(s) celda(s) de flujo en los puertos de acople del PromethION 24/48 de la siguiente manera:
- Alinearla con el conector (horizontal y verticalmente) e insertarla suavemente en la posición.
- Presionar con firmeza hasta que el cierre encaje y haga clic.


Si se inserta la celda de flujo en el ángulo equivocado existe el riesgo de dañar las clavijas del PromethION y afectar los resultados de secuenciación. Si observa que las clavijas de las posiciones del PromethION están dañadas, contacte con el servicio de asistencia en support@nanoporetech.com.

Antes de cargar la biblioteca, verificar la celda de flujo y determinar el número de poros disponible.
Este paso se puede omitir si se ha verificado la celda de flujo con anterioridad.
Encontrará más información en el documento Flow cell check.
Deslizar la tapa del puerto de entrada en el sentido de las agujas del reloj.

Tenga cuidado al extraer el amortiguador. No retire más de 20-30 μl y compruebe que cubra la matriz de poros en todo momento. La introducción de burbujas de aire en la matriz puede dañar los poros de manera irreversible.
Tras abrir el puerto de entrada, retirar una pequeña cantidad de amortiguador para quitar las burbujas de aire:
- Ajustar una pipeta P1000 a 200 μl.
- Introducir la punta en el puerto de entrada.
- Girar la rueda hasta que el indicador de volumen marque 220-230 μl o hasta que se pueda ver una pequeña cantidad entrar en la punta.

Cargar 500 μl de mezcla de acondicionamiento por el puerto de entrada, evitando introducir burbujas de aire. Esperar cinco minutos. Durante este tiempo, preparar la biblioteca siguiendo los siguientes pasos del protocolo.

Mezclar minuciosamente con la pipeta el contenido del vial Library Beads (LIB).
El vial Library Beads (LIB) contiene microesferas en suspensión. Las microesferas sedimentan muy rápido; por eso es crucial mezclarlas justo antes de su uso.
Recomendamos utilizar Library Beads (LIB) en la mayoría de experimentos de secuenciación. No obstante, el reactivo Library Solution (LIS) está disponible en caso de que se utilicen bibliotecas más viscosas.
En un tubo Eppendorf DNA LoBind de 1,5 ml preparar la biblioteca de la siguiente manera:
| Reactivo | Volumen por celda de flujo |
|---|---|
| Sequencing Buffer (SB) | 100 µl |
| Library Beads (LIB) bien mezclado antes de su uso o Library Solution (LIS) | 68 µl |
| Biblioteca de ADN | 32 µl |
| Total | 200 µl |
Nota: hemos aumentado el volumen de carga de la biblioteca, a fin de mejorar la cobertura de la matriz.
Terminar de acondicionar la celda de flujo cargando lentamente 500 µl de mezcla de preparación por el puerto de entrada.

Mezclar la biblioteca suavemente con la pipeta antes de cargarla.
Cargar 200 μl de biblioteca con una pipeta p1000.

Cerrar la válvula y sellar el puerto de entrada.
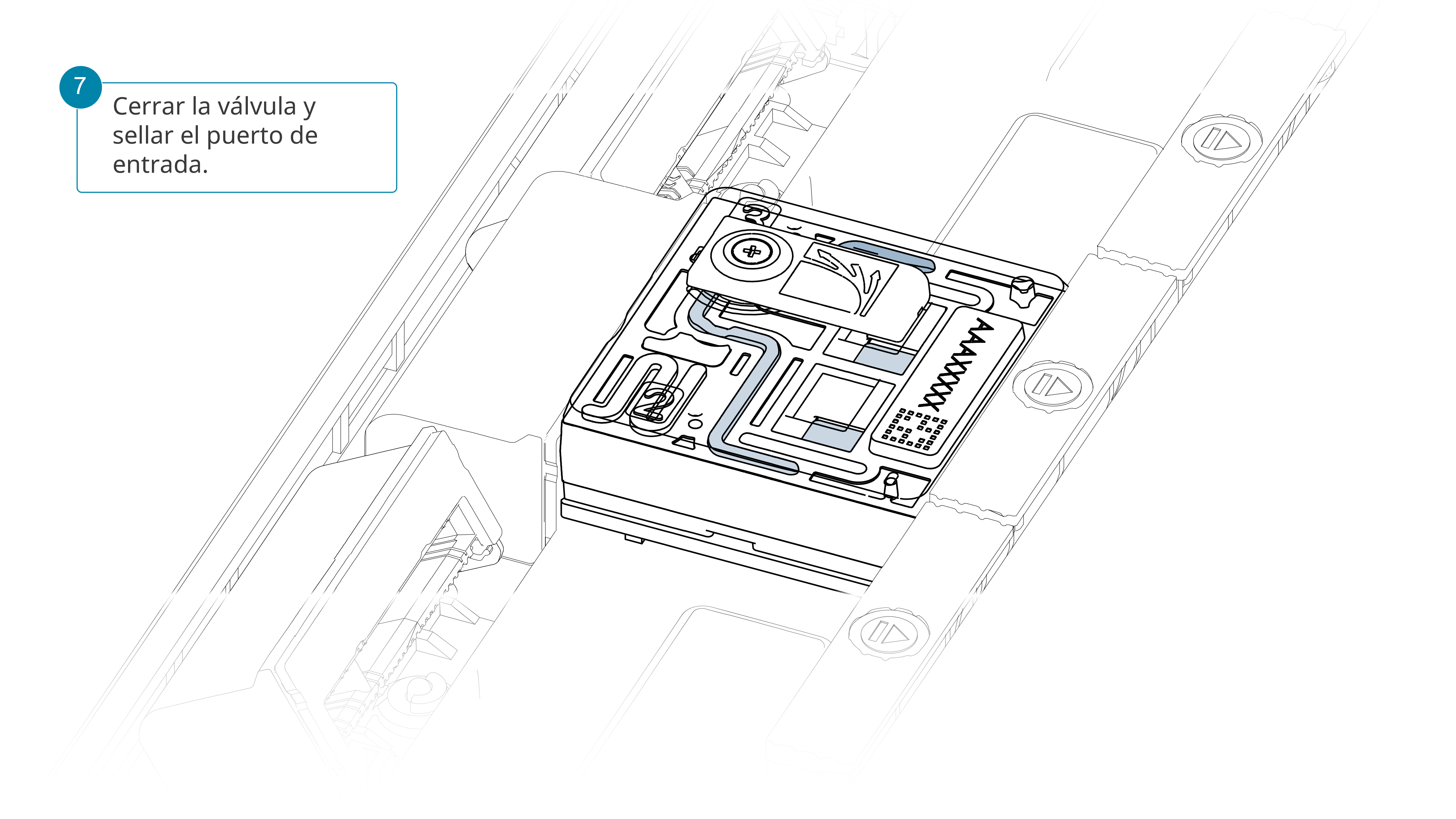
Colocar la pantalla protectora sobre la celda de flujo en cuanto se haya cargado la biblioteca favorecerá un rendimiento de secuenciación óptimo.
Recomendamos no retirarla mientras la biblioteca esté cargada ni durante los lavados o recargas. Se retira una vez se haya extraído la biblioteca.
Si se ha retirado, se instala de la siguiente manera:
- Alinear la abertura de la pantalla con la tapa del puerto de entrada. El borde delantero de la pieza debe quedar por encima del identificador de la celda de flujo.
- Presionar la pantalla protectora con firmeza. Cuando el clip del puerto de entrada encaje bajo la tapa del mismo, se producirá un clic.
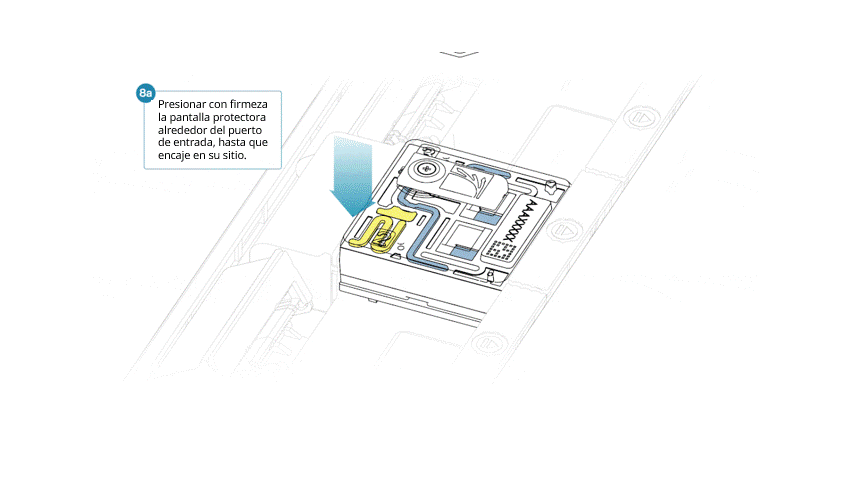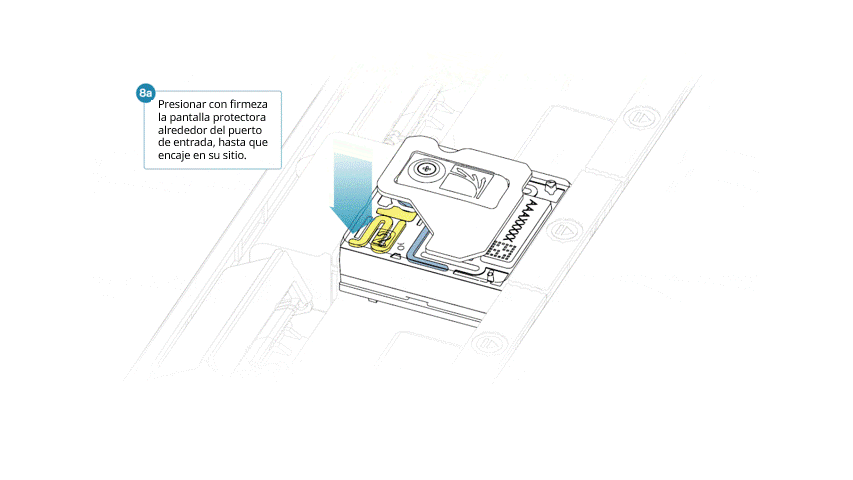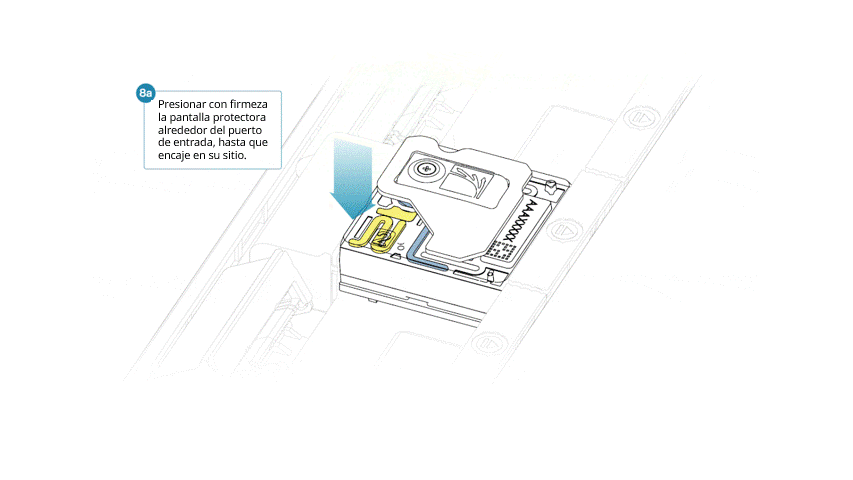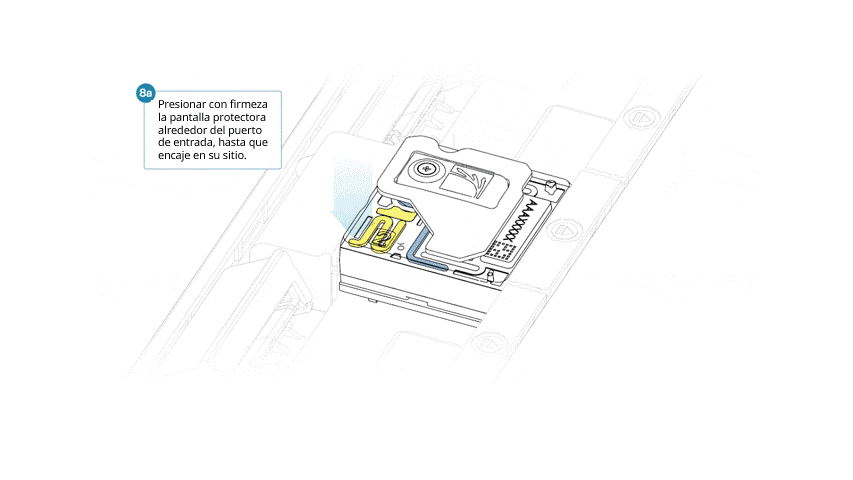
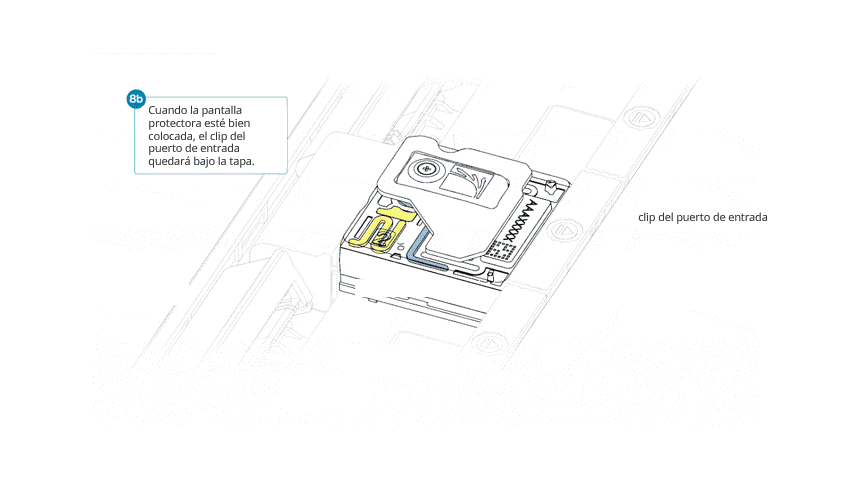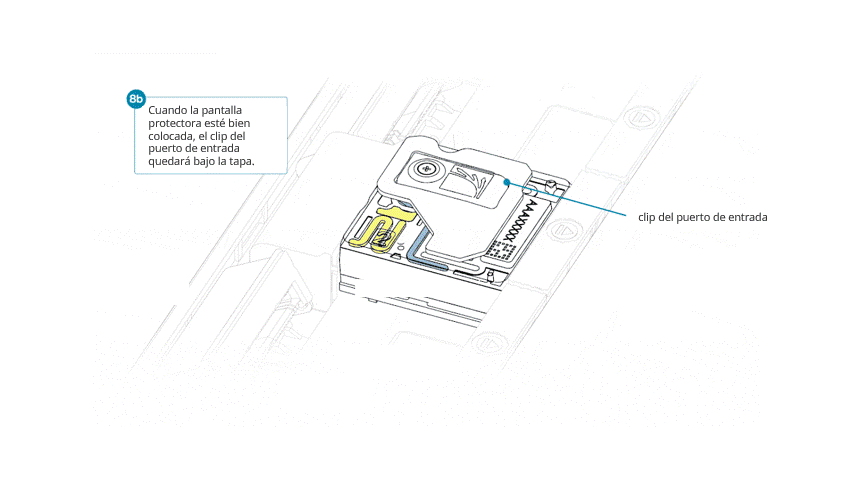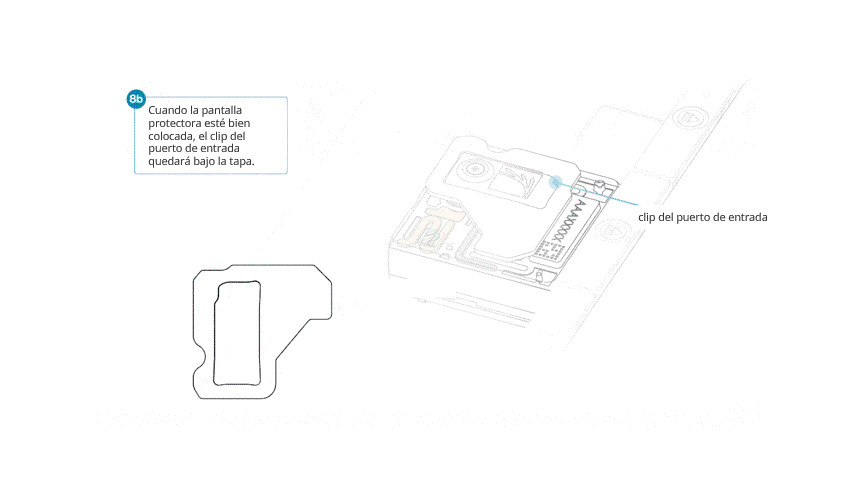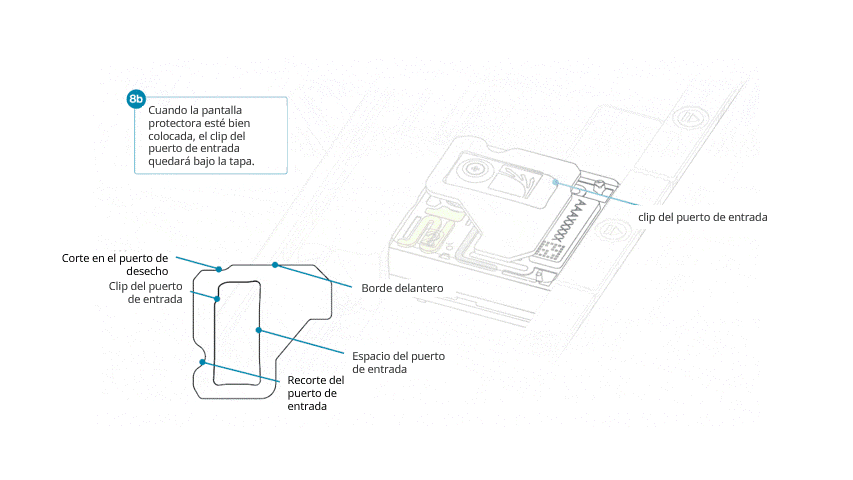
Cerrar la tapa del PromethION cuando esté listo para empezar un experimento de secuenciación en MinKNOW.
Tras cargar las celdas de flujo en el PromethION, esperar al menos 10 minutos antes de iniciar un experimento ayudará a aumentar el rendimiento de la secuenciación.
7. Adquisición de datos e identificación de bases
No recomendamos secuenciar y analizar los datos a la vez.
A fin de que la capacidad de procesamiento mantenga el ritmo de las exigencias de secuenciación o análisis, desaconsejamos ejecutar ambos procesos al mismo tiempo.
Compruebe que el/los experimento(s) de secuenciación haya(n) finalizado antes de empezar el análisis de datos. El análisis de datos se llevará a cabo tras la secuenciación.
Del mismo modo, no recomendamos empezar un experimento de secuenciación mientras el dispositivo esté analizando datos.
Utilice la versión más reciente de MinKNOW.
Recomendamos actualizar MinKNOW antes de empezar un experimento.
Dispone de instrucciones de actualización en el protocolo de MinKNOW.]
Cómo empezar a secuenciar
El programa MinKNOW gestiona el dispositivo de secuenciación y la adquisición de datos. Compruebe que MinKNOW esté instalado en su ordenador o dispositivo. Encontrará instrucciones adicionales para configurar experimentos de secuenciación en el Protocolo de MinKNOW.
Recomendamos configurar el experimento de secuenciación con las recomendaciones indicadas a continuación. Los demás parámetros se dejan en su configuración predeterminada.
Configuración de MinKNOW
Estas son las recomendaciones de configuración de MinKNOW:
Posiciones
Posición de celda de flujo: [Definida por el usuario]
Nombre del experimento: [definido por el usuario]
Tipo de celda de flujo: FLO-PRO114M
ID de muestra: [definido por el usuario]
Kit
Seleccionar el kit: Ligation Sequencing Kit (SQK-LSK114)
Configuración del experimento
Secuenciación y análisis
Identificación de bases: Encendido
Bases modificadas: Apagado [predeterminado]
Modelo: Identificación de bases de máxima precisión (SUP)
*\ Nota: si se ejecutan varias celdas de flujo a la vez, recomendamos utilizar la identificación de bases de gran precisión (HAC) y volver a identificarlas con SUP al finalizar el experimento.
Etiquetado con códigos de barras: Apagado [predeterminado]
Alineamiento: Apagado [predeterminado]
Muestreo adaptativo: Apagado [predeterminado]
Opciones avanzadas
Intervalo entre exploraciones de poros: 1,5 [predeterminado]
Reservar poros: Encendido [predeterminado]
Objetivos de datos
Duración máxima de la ejecución: detener el experimento cuando la secuenciación alcance 72 h
Salida
Formatos de salida
.BAM: Apagado
.FASTQ: Apagado
Lecturas sin procesar: Encendido [predeterminado]
.POD5: Encendido [predeterminado]
Filtrado: Encendido [predeterminado]
Índice Q score: 8 [predeterminado]
Longitud mínima de lectura: 200 b
Análisis de datos
Al finalizar la secuenciación, es posible reutilizar o devolver la celda de flujo, tal como se describe en la sección Reutilización y devolución de celdas de flujo.
Una vez la identificación de bases y la secuenciación han finalizado, se analizan los datos tal como se describe en la sección Análisis de datos.
8. Reutilización y devolución de celdas de flujo
Material
- Kit Flow Cell Wash (EXP-WSH004)
Al terminar el experimento, si quiere reutilizar la celda de flujo, siga las instrucciones del protocolo Flow Cell Wash Kit y guárdela a entre 2 °C y 8 °C.
El protocolo Flow Cell Wash Kit está disponible en la comunidad Nanopore.
Otra opción es seguir el procedimiento de devolución y enviarla de vuelta a Oxford Nanopore.
Ante cualquier problema o duda acerca del experimento de secuenciación, consulte la sección Resolución de problemas de la versión en línea de este protocolo.
9. Análisis de datos
Análisis de datos de secuenciación transcriptómica de células individuales a partir de ADNc 5’
Los archivos de salida (FASTQ o BAM) se analizan con wf-single-cell, un flujo de trabajo bioinformático desarrollado en Nextflow que forma parte de la plataforma de análisis de datos EPI2ME de Oxford Nanopore Technologies. El flujo de trabajo wf-single-cell está diseñado para ejecutarse desde la línea de comandos y desde la aplicación EPI2ME Desktop Application. wf-single-cell está disponible en GitHub.
Cómo ejecutar wf-single-cell
Ejecución del flujo de trabajo desde la línea de comandos:
nextflow run epi2me-labs/wf-single-cell \
--expected_cells <CELL NUMBER> \
--fastq <READS> \
--kit <KIT> \
--ref_genome_dir <REFERENCE> \
-profile standard
expected _cells corresponde al número de células seleccionadas en el experimento con 10x Chromium, fastq (o bam) a la ubicación de las lecturas identificadas, kit corresponde al kit y la versión de 10x utilizados (p. ej. 5prime:v4) y ref_genome_dir a la ubicación del genoma de referencia y los archivos de anotación de acuerdo con el formato de referencia 10x (encontrará más información en el centro de descargas de 10x.
La ejecución del flujo de trabajo requiere tener instalado Nextflow, Docker o Singularity en el sistema. Encontrará información adicional sobre cómo ejecutar los flujos de trabajo de EPI2ME desde la línea de comandos en la Guía de inicio rápido.
En la página de GitHub y en la documentación del flujo de trabajo se encuentra la información más reciente, junto con datos adicionales sobre cómo ejecutarlo y sobre los parámetros disponibles.
Archivos de salida
El flujo de trabajo wf-single-cell genera un informe interactivo en formato HTML, que incluye parámetros básicos de control de calidad (puntuación de secuenciación, longitudes de lectura), un resumen del experimento (número de células, media de lecturas por célula, etc.), gráficos diagnósticos de saturación y gráfico de inflexión, así como gráficos UMAP que representan los agrupamientos celulares. También genera matrices de expresión génica y de transcritos en un formato compatible con las herramientas de análisis más utilizadas.
10. Problemas durante la extracción de ADN y preparación de la biblioteca
A continuación hay una lista de los problemas más frecuentes, con algunas posibles causas y soluciones propuestas.
También disponemos de una sección de preguntas frecuentes (FAQ) en la sección Support de la comunidad Nanopore.
Si ha probado las soluciones propuestas y los problemas aún persisten, póngase en contacto con el departamento de Asistencia técnica, bien por correo electrónico (support@nanoporetech.com) o a través del chat Live Support de la comunidad Nanopore.
Baja calidad de la muestra
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Baja pureza del ADN (la lectura del Nanodrop del ADN con una relación OD 260/280 es <1,8 y OD 260/230 es <2,0-2,2) | El método de extracción de ADN no proporciona la pureza necesaria | Los efectos de los contaminantes se muestran en el documento Contaminants. Probar con otro método de extracción que no provoque el arrastre de contaminantes. Considere realizar un paso adicional de limpieza SPRI. |
Escasa recuperación de ADN tras la limpieza con microesferas AMPure
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Escasa recuperación | Pérdida de ADN debido a una proporción de microesferas AMPure por muestra inferior a lo previsto. | 1. Las microesferas AMPure precipitan con rapidez; antes de añadirlas a la muestra deben estar bien resuspendidas. 2. Si la proporción de microesferas AMPure por muestra es inferior a 0.4:1, los fragmentos de ADN, sean del tamaño que sean, se perderán durante la limpieza. |
| Escasa recuperación | Los fragmentos de ADN son más cortos de lo esperado | Cuanto menor sea la proporción de microesferas AMPure por muestra, más rigurosa será la selección de fragmentos largos frente a los cortos. Determinar siempre la longitud de la muestra de ADN en un gel de agarosa u otros métodos de electroforesis en gel y a continuación, calcular la cantidad adecuada de microesferas AMPure que se debe utilizar. 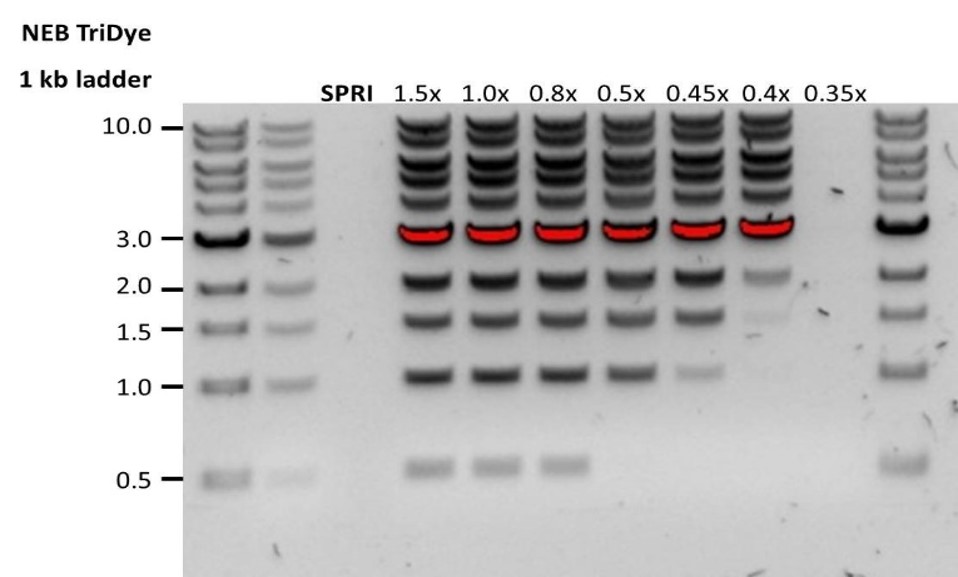 |
| Escasa recuperación tras la preparación de extremos | En el paso de lavado se utilizó etanol en una concentración inferior al 70 % | Si se utiliza etanol a una concentración inferior al 70 %, el ADN se eluye de las microesferas. Utilice el porcentaje correcto. |
11. Problemas durante el experimento de secuenciación
A continuación hay una lista de los problemas más frecuentes, con algunas posibles causas y soluciones propuestas.
También dispone de una sección de preguntas frecuentes, en la sección Support de la comunidad Nanopore.
Si ha probado las soluciones propuestas y los problemas aún persisten, póngase en contacto con el departamento de Asistencia técnica, bien por correo electrónico (support@nanoporetech.com) o a través del chat de la comunidad Nanopore.
Menos poros al inicio de la secuenciación que tras la evaluación de la celda de flujo
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la evaluación de la celda de flujo. | Se introdujo una burbuja de aire en la matriz de nanoporos. | Tras comprobar el número de poros presente en la celda de flujo y antes de acondicionarla, es imprescindible quitar las burbujas de aire que haya cerca del puerto de purgado. Si no se quitan, las burbujas pueden desplazarse a la matriz de poros y dañar de manera irreversible los nanoporos expuestos al aire. En el vídeo Cómo cargar una celda de flujo PromethION se muestran algunas buenas prácticas para evitar que esto ocurra. |
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la comprobación de la celda de flujo. | La celda de flujo no está colocada correctamente. | Detener el ciclo de secuenciación, quitar la celda de flujo del dispositivo e insertarla de nuevo. Comprobar que está firmemente asentada y que ha alcanzado la temperatura deseada. Si procede, probar a insertarla en una posición diferente. |
| MinKNOW presentó al inicio de la secuenciación un número de poros inferior al indicado durante la evaluación de la celda de flujo | La presencia de contaminantes en la biblioteca ha dañado o bloqueado los poros. | El recuento de poros durante la evaluación de la celda de flujo se efectúa utilizando las moléculas de ADN del control de calidad presentes en el amortiguador de almacenamiento. Al inicio de la secuenciación, se utiliza la misma biblioteca para calcular el número de poros activos. Por este motivo, se estima que existe una variabilidad del 10 % en el número de poros detectados. Tener un número de poros considerablemente inferior al inicio de la secuenciación suele estar relacionado con la presencia de contaminantes en la biblioteca que hayan dañado las membranas o bloqueado los poros. En algunos casos, se recomienda emplear métodos alternativos de extracción o purificación de ADN/ARN para mejorar la pureza del material de partida. Los efectos de los contaminantes se muestran en la página Contaminants. Probar con un método de extracción diferente que no provoque el arrastre de contaminantes. |
Error en el script de MinKNOW
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW muestra el mensaje "Error en el script" | Reiniciar el ordenador y reiniciar MinKNOW. Si el problema persiste, reúna los archivos de registro de MinKNOW y contacte con el departamento de Asistencia técnica. Si no dispone de otro dispositivo de secuenciación, recomendamos que guarde la celda de flujo cargada a 4 °C y contacte con el servicio de asistencia técnica, que proporcionará instrucciones de almacenamiento adicionales. |
Ocupación de poro por debajo del 40 %
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Ocupación de poro inferior al 40 % | No se cargó suficiente cantidad de biblioteca en la celda de flujo | Cargue la biblioteca al volumen y la concentración adecuados, tal como se indica en el protocolo correspondiente. Es necesario cuantificar la biblioteca antes de cargarla y calcular los moles con herramientas como la calculadora Biomath de Promega, seleccionando la opción "dsDNA: μg to pmol". |
| Ocupación de poro próxima a 0 | Se utilizó el kit Ligation Sequencing y los adaptadores de secuenciación no se ligaron al ADN | En la fase de ligación del adaptador, añadir la cantidad recomendada de NEBNext Quick Ligation Module (E6056) y el amortiguador Ligation Buffer (LNB) suministrado en el kit. Preparar una biblioteca de control con lambda para valorar la integridad de los reactivos de otros fabricantes. |
| Ocupación de poro próxima a 0 | Se utilizó el kit Ligation Sequencing y en la fase de lavado, después de ligar el adaptador, se utilizó etanol en lugar de Long Fragment Buffer (LFB) o Short Fragment Buffer (SFB). | El etanol puede desnaturalizar la proteína motor en los adaptadores de secuenciación. Usar Long Fragment Buffer (LFB) o Short Fragment Buffer (SFB) después de la ligación de los adaptadores. |
| Ocupación de poro próxima a 0 | No hay anclaje en la celda de flujo | Los anclajes se añaden durante el acondicionamiento de la celda de flujo (viales (FLT)/(FCT)). Añadir Flush Tether (FLT) o Flow Cell Tether (FCT) al vial Flush Buffer (FB) o Flow cell Flush (FCF) antes de acondicionar la celda de flujo. |
Longitud de lectura más corta de lo esperado
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Longitud de lectura más corta de lo esperado | Fragmentación no deseada de la muestra de ADN | La longitud de lectura refleja la longitud del fragmento de la muestra de ADN. La fragmentacion tiene lugar durante los procesos de extracción y preparación de la biblioteca. 1. Consulte la sección de buenas prácticas de extracción en la página Extraction Methods de la comunidad Nanopore. 2. Visualizar la distribución de la longitud de los fragmentos de las muestras de ADN en un gel de agarosa antes de proceder a la preparación de la biblioteca. 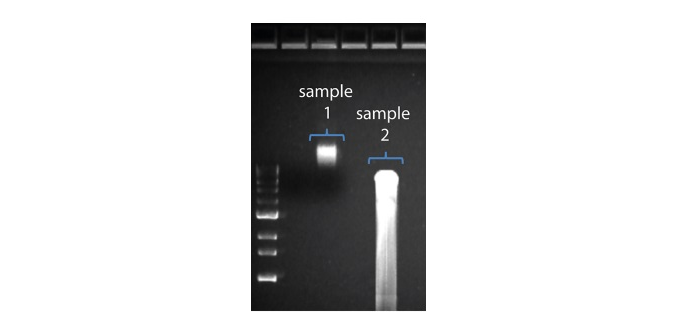 En la imagen superior, la muestra 1 contiene un elevado peso molecular, mientras que la muestra 2 se ha fragmentado. En la imagen superior, la muestra 1 contiene un elevado peso molecular, mientras que la muestra 2 se ha fragmentado.3. Durante la preparación de la biblioteca, evite pipetear y agitar en vórtex al mezclar los reactivos. Dar suaves golpes con el dedo o invertir el vial es suficiente. |
Gran proporción de poros no disponibles
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
Gran proporción de poros no disponibles (se muestran en azul en el panel de canales y en el gráfico de actividad de poros) 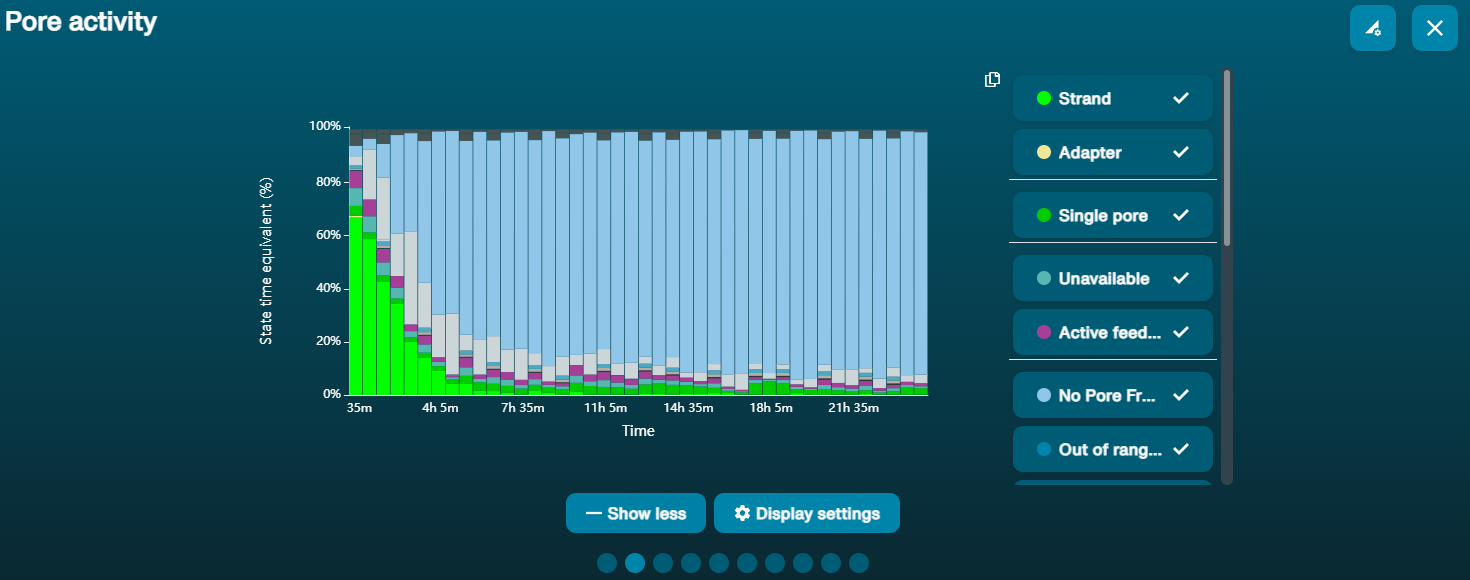 El gráfico de actividad de poros de arriba muestra una proporción creciente de poros "no disponibles». El gráfico de actividad de poros de arriba muestra una proporción creciente de poros "no disponibles». | Hay contaminantes presentes en la muestra | Algunos contaminantes se pueden eliminar de los poros mediante la función de desbloqueo incorporada en MinKNOW. Si funciona, el estado de los poros cambiará a "sequencing pores". Si la porción de poros no disponibles se mantiene elevada o aumenta: 1. Es posible realizar un lavado con nucleasa utilizando el kit Flow Cell Wash (EXP-WSH004), o 2. Realizar varios ciclos de PCR a fin de diluir cualquier contaminante que esté causando problemas. |
Gran proporción de poros inactivos
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Gran proporción de poros inactivos o no disponibles (se muestran en azul claro en el panel de canales y en el gráfico de actividad de poros). Los poros o membranas han sufrido daños irreversibles) | Se han introducido burbujas de aire en la celda de flujo | Las burbujas de aire introducidas durante el acondicionamiento de la celda y carga de la biblioteca provocan daños permanentes. La forma más eficaz de evitar que esto ocurra se muestra en el vídeo Cómo cargar celdas de flujo PromethION. |
| Gran proporción de poros inactivos o no disponibles | Hay contaminantes presentes en la muestra | Los efectos de los contaminantes se muestran en el documento Contaminants. Probar con un método de extracción alternativo que no provoque el arrastre de contaminantes. |
Fluctuación de la temperatura
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| Fluctuación de la temperatura | La celda de flujo ha perdido contacto con el dispositivo | Comprobar que una almohadilla térmica cubra la placa metálica de la parte posterior de la celda de flujo. Reinsertar la celda de flujo y presionar hasta que las clavijas del conector estén firmemente en contacto con el dispositivo. Si el problema persiste, contacte con el servicio de Asistencia técnica. |
Error al intentar alcanzar la temperatura deseada
| Observaciones | Posibles causas | Comentarios y acciones recomendadas |
|---|---|---|
| MinKNOW muestra el mensaje «Error al intentar alcanzar la temperatura deseada» | El dispositivo se colocó en una ubicación con una temperatura ambiente inferior a la media o con escasa ventilación (lo que provoca el sobrecalientamiento de las celdas de flujo). | MinKNOW establece un tiempo para que la celda de flujo alcance la temperatura fijada. Si se supera el tiempo establecido, aparecerá un mensaje de error, pero el experimento de secuenciación continuará. Secuenciar a una temperatura incorrecta puede llevar a una disminución en el rendimiento y generar índices de calidad Q score menores. Ajuste la ubicación del dispositivo, procurando que esté a temperatura ambiente y con buena ventilación y reinicie la secuenciación en MinKNOW. |







